2.下列离子方程式中,正确的是( )
| A. | 向Mg(HCO3)2溶液中加入过量的NaOH溶液Mg2++2HCO3-+2OH-═MgCO3↓+CO32-+2H2O | |
| B. | 溴化亚铁溶液中通入足量的氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| C. | 少量的CO2通入稀的碳酸钠溶液中:CO2+CO32-+H2O═2HCO3- | |
| D. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO42-反应完全2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O |
1.水是一种战略性经济资源,下列物质对水质不会产生严重污染的是( )
| A. | CH3OH | B. | SO2 | C. | HgCl2 | D. | CO2 |
20.为验证氧化性:Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕)
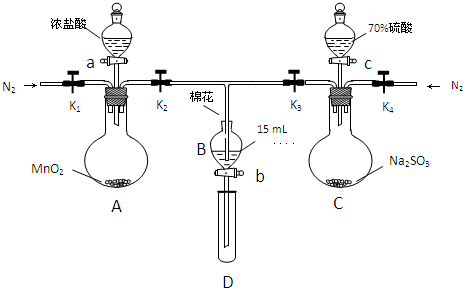
实验过程:
Ⅰ.打开弹簧夹K1-K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中的溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2ml的溶液流入D试管中,检验其中的离子.
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
Ⅵ.更新试管D,重复过程IV,检验B溶液中的离子.
(1)过程Ⅰ的目的是排出装置中的氧气
(2)棉花中浸润的溶液为氢氧化钠溶液
(3)A中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O
(4)用70%的硫酸支取SO2,反应速率比用98%的硫酸块,原因是70%的硫酸中的H+的浓度比98%的硫酸中的H+的浓度大
(5)过程Ⅳ中检验B溶液中是否含有硫酸根的操作是取少量B溶液于试管中,加入足量的稀盐酸酸化,在滴加几滴氯化钡溶液,若有白色沉淀生成,证明溶液B中有硫酸根
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化Cl2>Fe3+>SO2的是乙丙
(7)进行实验过程Ⅴ时,B中的溶液颜色由黄色变为红棕色,停止通气,放置一段时间后溶液颜色变为浅绿色.
查阅资料:Fe2+(aq)+SO32-(aq)?FeSO3(s)
提出假设:FeCl3和SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合颜色.
某同学设计如下实验,证实该假设的成立:
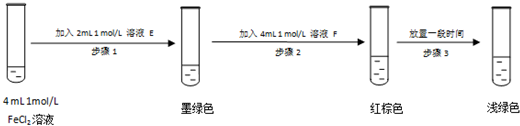
溶液E和F分别是Na2SO3溶液、FeCl3溶液
请用化学平衡原理解释步骤3红棕色溶液变为浅绿色的原因反应2Fe3++SO32-+H2O=2Fe2++SO42-+2H+,促使Fe3++3H2O Fe(OH)3+3H+和SO32-+H2O
Fe(OH)3+3H+和SO32-+H2O  HSO32-+OH-逆向进行,溶液变为浅绿色.
HSO32-+OH-逆向进行,溶液变为浅绿色.

实验过程:
Ⅰ.打开弹簧夹K1-K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中的溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2ml的溶液流入D试管中,检验其中的离子.
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
Ⅵ.更新试管D,重复过程IV,检验B溶液中的离子.
(1)过程Ⅰ的目的是排出装置中的氧气
(2)棉花中浸润的溶液为氢氧化钠溶液
(3)A中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O
(4)用70%的硫酸支取SO2,反应速率比用98%的硫酸块,原因是70%的硫酸中的H+的浓度比98%的硫酸中的H+的浓度大
(5)过程Ⅳ中检验B溶液中是否含有硫酸根的操作是取少量B溶液于试管中,加入足量的稀盐酸酸化,在滴加几滴氯化钡溶液,若有白色沉淀生成,证明溶液B中有硫酸根
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化Cl2>Fe3+>SO2的是乙丙
| 过程ⅣB溶液中含有的离子 | 过程ⅥB溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查阅资料:Fe2+(aq)+SO32-(aq)?FeSO3(s)
提出假设:FeCl3和SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合颜色.
某同学设计如下实验,证实该假设的成立:

溶液E和F分别是Na2SO3溶液、FeCl3溶液
请用化学平衡原理解释步骤3红棕色溶液变为浅绿色的原因反应2Fe3++SO32-+H2O=2Fe2++SO42-+2H+,促使Fe3++3H2O
 Fe(OH)3+3H+和SO32-+H2O
Fe(OH)3+3H+和SO32-+H2O  HSO32-+OH-逆向进行,溶液变为浅绿色.
HSO32-+OH-逆向进行,溶液变为浅绿色.
16.有文献记载:在强碱条件下,加热银氨溶液可能析出银镜.某同学进行如下验证和对比实验.
该同学欲分析实验Ⅰ和实验Ⅱ的差异,查阅资料:
a.Ag(NH3)2++2H2O=Ag++2NH3+H2O b.AgOH不稳定,极易分解为黑色Ag2O
(1)配制银氨溶液所需的药品是AgNO3溶液和浓氨水.
(2)经检验,实验Ⅰ的气体中有NH3,黑色物质中有Ag2O.
①用湿润的红色石蕊试纸检验NH3,产生的现象是试纸变蓝.
②产生Ag2O的原因是在NaOH存在下,加热促进NH3•H2O分解,逸出NH3,促使平衡Ag(NH3)2++2H2O?Ag++2NH3•H2O正向移动,c(Ag+)增大,Ag+与OH-反应2OH-+2Ag+=Ag2O+H2O,立即转化为Ag2O.
(3)该同学对产生银镜的原因提出假设:可能是NaOH还原Ag2O.实验及现象:向AgNO3溶液中加入过量NaOH溶液,出现黑色沉淀;水浴加热,未出现银镜.
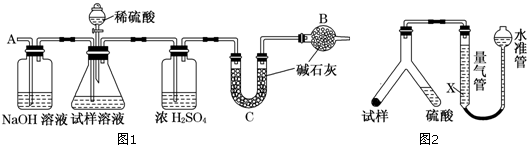
(4)重新假设:在NaOH存在下.可能是NH3,还原Ag2O.用图1所示装置进行实验.现象:出现银镜.在虚线框内画出用生石灰和浓氨水制取NH3的装置简图(夹持仪器略).

(5)该同学认为在(4)的实验中会有Ag(NH3)2OH生成.由此又提出假设:在NaOH存在下,可能是Ag
(NH3)2OH也参与了NH3还原Ag2O的反应.进行如图2的实验:
①有部分Ag2O溶解在氨水中,该反应的化学方程式是Ag2O+4 NH3•H2O=2Ag(NH3)2OH+3H2O.
②实验结果证实假设成立,依据的现象是与溶液接触的试管壁上析出银镜.
(6)用HNO3消洗试管壁上的Ag,该反应的化学方程式是4HNO3(稀)+3Ag═3AgNO3+NO↑+2H2O.
| 装置 | 实验序号 | 试管中的药品 | 现象 |
 | 实验Ⅰ | 2mL银氨溶液和数 滴较浓NaOH溶液 | 有气泡产生: 一段时间后,溶液 逐渐变黑:试管壁 附着银镜 |
| 实验Ⅱ | 2mL银氮溶液和 数滴浓氨水 | 有气泡产生: 一段时间后,溶液 无明显变化 |
a.Ag(NH3)2++2H2O=Ag++2NH3+H2O b.AgOH不稳定,极易分解为黑色Ag2O
(1)配制银氨溶液所需的药品是AgNO3溶液和浓氨水.
(2)经检验,实验Ⅰ的气体中有NH3,黑色物质中有Ag2O.
①用湿润的红色石蕊试纸检验NH3,产生的现象是试纸变蓝.
②产生Ag2O的原因是在NaOH存在下,加热促进NH3•H2O分解,逸出NH3,促使平衡Ag(NH3)2++2H2O?Ag++2NH3•H2O正向移动,c(Ag+)增大,Ag+与OH-反应2OH-+2Ag+=Ag2O+H2O,立即转化为Ag2O.
(3)该同学对产生银镜的原因提出假设:可能是NaOH还原Ag2O.实验及现象:向AgNO3溶液中加入过量NaOH溶液,出现黑色沉淀;水浴加热,未出现银镜.
(4)重新假设:在NaOH存在下.可能是NH3,还原Ag2O.用图1所示装置进行实验.现象:出现银镜.在虚线框内画出用生石灰和浓氨水制取NH3的装置简图(夹持仪器略).

(5)该同学认为在(4)的实验中会有Ag(NH3)2OH生成.由此又提出假设:在NaOH存在下,可能是Ag
(NH3)2OH也参与了NH3还原Ag2O的反应.进行如图2的实验:
①有部分Ag2O溶解在氨水中,该反应的化学方程式是Ag2O+4 NH3•H2O=2Ag(NH3)2OH+3H2O.
②实验结果证实假设成立,依据的现象是与溶液接触的试管壁上析出银镜.
(6)用HNO3消洗试管壁上的Ag,该反应的化学方程式是4HNO3(稀)+3Ag═3AgNO3+NO↑+2H2O.
14.25℃、1.01×105Pa,下列哪个反应放出的热量表示乙炔的燃烧热(单位:kj•mol-1)( )
0 154081 154089 154095 154099 154105 154107 154111 154117 154119 154125 154131 154135 154137 154141 154147 154149 154155 154159 154161 154165 154167 154171 154173 154175 154176 154177 154179 154180 154181 154183 154185 154189 154191 154195 154197 154201 154207 154209 154215 154219 154221 154225 154231 154237 154239 154245 154249 154251 154257 154261 154267 154275 203614
| A. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g) | B. | C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(1) | ||
| C. | C2H2(g)+$\frac{3}{2}$O2(g)=2CO2(g)+H2O(g) | D. | C2H2(g)+$\frac{3}{2}$O2(g)=2CO(g)+H2O(1) |