题目内容
1.水是一种战略性经济资源,下列物质对水质不会产生严重污染的是( )| A. | CH3OH | B. | SO2 | C. | HgCl2 | D. | CO2 |
分析 对水质不产生严重污染,不能像水中排放污染物,如甲醇、硫氧化物、氮氧化物以及重金属盐,以此解答该题.
解答 解:题中CH3OH、SO2都是有害物质,对人体有害,PbCl2为重金属盐,对人体有害,不能排放到水中,CO2微溶于水,对水质不会产生严重污染.
故选D.
点评 本题考查常见环境污染及治理,为高频考点,侧重于化学与环境的考查,有利于培养学生良好的科学素养,题目难度不大,注意相关物质的性质,把握常见物质的性质以及对环境的危害.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
16.有文献记载:在强碱条件下,加热银氨溶液可能析出银镜.某同学进行如下验证和对比实验.
该同学欲分析实验Ⅰ和实验Ⅱ的差异,查阅资料:
a.Ag(NH3)2++2H2O=Ag++2NH3+H2O b.AgOH不稳定,极易分解为黑色Ag2O
(1)配制银氨溶液所需的药品是AgNO3溶液和浓氨水.
(2)经检验,实验Ⅰ的气体中有NH3,黑色物质中有Ag2O.
①用湿润的红色石蕊试纸检验NH3,产生的现象是试纸变蓝.
②产生Ag2O的原因是在NaOH存在下,加热促进NH3•H2O分解,逸出NH3,促使平衡Ag(NH3)2++2H2O?Ag++2NH3•H2O正向移动,c(Ag+)增大,Ag+与OH-反应2OH-+2Ag+=Ag2O+H2O,立即转化为Ag2O.
(3)该同学对产生银镜的原因提出假设:可能是NaOH还原Ag2O.实验及现象:向AgNO3溶液中加入过量NaOH溶液,出现黑色沉淀;水浴加热,未出现银镜.
(4)重新假设:在NaOH存在下.可能是NH3,还原Ag2O.用图1所示装置进行实验.现象:出现银镜.在虚线框内画出用生石灰和浓氨水制取NH3的装置简图(夹持仪器略).

(5)该同学认为在(4)的实验中会有Ag(NH3)2OH生成.由此又提出假设:在NaOH存在下,可能是Ag
(NH3)2OH也参与了NH3还原Ag2O的反应.进行如图2的实验:
①有部分Ag2O溶解在氨水中,该反应的化学方程式是Ag2O+4 NH3•H2O=2Ag(NH3)2OH+3H2O.
②实验结果证实假设成立,依据的现象是与溶液接触的试管壁上析出银镜.
(6)用HNO3消洗试管壁上的Ag,该反应的化学方程式是4HNO3(稀)+3Ag═3AgNO3+NO↑+2H2O.
| 装置 | 实验序号 | 试管中的药品 | 现象 |
 | 实验Ⅰ | 2mL银氨溶液和数 滴较浓NaOH溶液 | 有气泡产生: 一段时间后,溶液 逐渐变黑:试管壁 附着银镜 |
| 实验Ⅱ | 2mL银氮溶液和 数滴浓氨水 | 有气泡产生: 一段时间后,溶液 无明显变化 |
a.Ag(NH3)2++2H2O=Ag++2NH3+H2O b.AgOH不稳定,极易分解为黑色Ag2O
(1)配制银氨溶液所需的药品是AgNO3溶液和浓氨水.
(2)经检验,实验Ⅰ的气体中有NH3,黑色物质中有Ag2O.
①用湿润的红色石蕊试纸检验NH3,产生的现象是试纸变蓝.
②产生Ag2O的原因是在NaOH存在下,加热促进NH3•H2O分解,逸出NH3,促使平衡Ag(NH3)2++2H2O?Ag++2NH3•H2O正向移动,c(Ag+)增大,Ag+与OH-反应2OH-+2Ag+=Ag2O+H2O,立即转化为Ag2O.
(3)该同学对产生银镜的原因提出假设:可能是NaOH还原Ag2O.实验及现象:向AgNO3溶液中加入过量NaOH溶液,出现黑色沉淀;水浴加热,未出现银镜.
(4)重新假设:在NaOH存在下.可能是NH3,还原Ag2O.用图1所示装置进行实验.现象:出现银镜.在虚线框内画出用生石灰和浓氨水制取NH3的装置简图(夹持仪器略).

(5)该同学认为在(4)的实验中会有Ag(NH3)2OH生成.由此又提出假设:在NaOH存在下,可能是Ag
(NH3)2OH也参与了NH3还原Ag2O的反应.进行如图2的实验:
①有部分Ag2O溶解在氨水中,该反应的化学方程式是Ag2O+4 NH3•H2O=2Ag(NH3)2OH+3H2O.
②实验结果证实假设成立,依据的现象是与溶液接触的试管壁上析出银镜.
(6)用HNO3消洗试管壁上的Ag,该反应的化学方程式是4HNO3(稀)+3Ag═3AgNO3+NO↑+2H2O.
10.以下名称、化学用语均正确的是( )
| A. | 笨的实验式:CH | B. | 二氯乙稀的结构简式:CH2=C(Cl)2 | ||
| C. | 甲酸的结构式: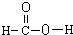 | D. | 醛基的电子式: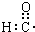 |
1.(1)配制物质的量浓度为0.20mol•L-1NaOH溶液500mL,请回答下列问题(在横线上填上相应答案):
(2)在配制上述溶液时,下列哪个原因会造成所配溶液浓度偏高( )
A.所用NaOH已经潮解
B.向容量瓶中加水未到刻度线
C.有少量NaOH溶液残留在烧杯里
D.称量时误用“左码右物”
| 应称量NaOH的质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
| 4.0 | 500 | 烧杯、量筒、玻璃棒、药匙、托盘天平、胶头滴管 |
A.所用NaOH已经潮解
B.向容量瓶中加水未到刻度线
C.有少量NaOH溶液残留在烧杯里
D.称量时误用“左码右物”
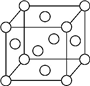 A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题:
A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题: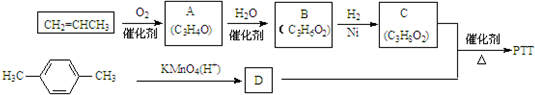
 .①分子式为C4H6O ②含有1个-CH3
.①分子式为C4H6O ②含有1个-CH3 ,反应类型为缩聚反应.
,反应类型为缩聚反应.