16.某恒容密闭容器中充入等物质的量的A 和B,一定温度下发生反应A(s)+xB(g)?2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
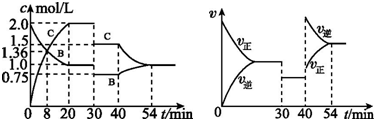
下列说法中正确的是( )

下列说法中正确的是( )
| A. | 30 min~40 min 间该反应使用了催化剂 | |
| B. | 反应方程式中的x=2,正反应为吸热反应 | |
| C. | 30 min 时条件的变化是降低压强,40 min 时条件的变化是升高温度 | |
| D. | 前8 min A 的平均反应速率为0.08 mol•L-1•min-1 |
15.下列叙述正确的是( )
| A. | 久置在空气中的NaOH溶液,加盐酸时有气体产生 | |
| B. | 50 mL 12 mol•L-1的浓盐酸与足量的MnO2反应,生成0.15 mol Cl2 | |
| C. | 在常温下,浓H2SO4不与Cu反应,是因为铜被钝化 | |
| D. | CO2通入浓的CaCl2溶液中产生白色沉淀 |
14.纤维素被称为第七营养素.食物中的纤维素虽然不能为人体提供能量,但能促进肠道蠕动、吸附排出有害物质.不能用于鉴别淀粉和纤维素的方法是( )
| A. | 分别加入碘水,观察颜色反应 | |
| B. | 分别加稀硫酸煮沸,再加足量NaOH溶液调至碱性,加银氨溶液加热观察有无银镜 | |
| C. | 分别加热水溶解,观察溶解性 | |
| D. | 放在嘴里咀嚼,有无甜味产生 |
13.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在1 L 2 mol•L-1的硝酸镁溶液中含有的硝酸根离子数为2NA | |
| B. | 2.3 g Na变成Na+时失去的电子数目为0.2NA | |
| C. | 1 mol H2O的质量与NA个H2O的质量之和相等 | |
| D. | 在通常状况下,22.4 L O2与N2的混合物所含分子数为NA |
12.在KIO3、KHSO3的酸性混合溶液中加入少量KI和淀粉,不停地搅拌,有下列反应发生:
①IO3-+5I-+6H+═3I2+3H2O;
②I2+HSO3-+H2O═21-+SO42-+3H+.
当反应进行到某一时间时,溶液突然变为蓝色,随之又很快消失,这一反应称作“时钟反应”,有人用它来解释生物钟现象.下列有关说法错误的是( )
①IO3-+5I-+6H+═3I2+3H2O;
②I2+HSO3-+H2O═21-+SO42-+3H+.
当反应进行到某一时间时,溶液突然变为蓝色,随之又很快消失,这一反应称作“时钟反应”,有人用它来解释生物钟现象.下列有关说法错误的是( )
| A. | ①②反应均是氧化还原反应 | |
| B. | KI在整个反应过程中起催化作用 | |
| C. | KI在整个反应过程中起氧化作用 | |
| D. | “溶液突然变为蓝色,随之又很快消失”这一现象与①②的反应速率有关 |
11.某化学兴趣小组的成员捡到一块矿石,观察外观发现该矿石坚硬且呈红褐色,投入水中没有任何变化,再向水中加浓盐酸至过量,矿石部分溶解,并有大量无色气体生成.学生猜测该矿石可能由CaCO3、SiO2、Fe2O3三种成分组成,试设计实验证明CaCO3以外的两种成分.
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、滴管、药匙、漏斗、漏斗架;2 mol•L-1盐酸、2mol•L-1NaOH溶液、2%的KSCN溶液.
(1)将实验方案用以下流程示意图表示,试写出每步所用试剂的名称或化学式.
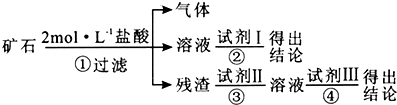
试剂Ⅰ2%的KSCN溶液;试剂Ⅱ2mol•L-1NaOH溶液;试剂Ⅲ2mol•L-1盐酸.
(2)如果猜测是成立的,试根据上述实验方案,叙述实验操作,预期现象和结论.
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、滴管、药匙、漏斗、漏斗架;2 mol•L-1盐酸、2mol•L-1NaOH溶液、2%的KSCN溶液.
(1)将实验方案用以下流程示意图表示,试写出每步所用试剂的名称或化学式.

试剂Ⅰ2%的KSCN溶液;试剂Ⅱ2mol•L-1NaOH溶液;试剂Ⅲ2mol•L-1盐酸.
(2)如果猜测是成立的,试根据上述实验方案,叙述实验操作,预期现象和结论.
| 编号 | 实验操作 | 预期现象和结论 |
| ① | 取适量矿石研细,加 足量2 mol•L-1盐酸 | 有大量无色气体生成,得棕黄 色溶液,且仍有少量固体残留 |
| ② | ||
| ③ | ||
| ④ |
9.科学家P.Tatapudi等人首先使用在空气中电解水(酸性条件下)的方法,在阳极制得臭氧,阴极制得过氧化氢.电解总方程式为:3H2O+3O2$\frac{\underline{\;电解\;}}{\;}$3H2O2+O3,下列说法正确的是( )
| A. | 电解产物在应用中都只能作为氧化剂 | |
| B. | 电解一段时间后,溶液pH不变 | |
| C. | 阳极反应:3H2O-6e-═O3+6H+ | |
| D. | 每生成1 mol O3转移电子数为3 mol |
8.配制250 mL 0.10 mol•L-1的NaOH溶液时,下列实验操作会使配制的溶液浓度偏高的是( )
0 154034 154042 154048 154052 154058 154060 154064 154070 154072 154078 154084 154088 154090 154094 154100 154102 154108 154112 154114 154118 154120 154124 154126 154128 154129 154130 154132 154133 154134 154136 154138 154142 154144 154148 154150 154154 154160 154162 154168 154172 154174 154178 154184 154190 154192 154198 154202 154204 154210 154214 154220 154228 203614
| A. | 容量瓶内有水,未经过干燥处理 | |
| B. | 定容时,仰视刻度线 | |
| C. | 用量筒量取浓NaOH溶液时,用水洗涤量筒2~3次,洗涤液倒入烧杯中 | |
| D. | 定容后倒转容量瓶几次,发现液体最低点低于刻度线,再补加几滴水到刻度线 |
 理论上任何自发的氧化还原反应都可以设计成原电池.现使用锌电极、铜电极、橙子(酸性介质)设计如图所示的水果电池.
理论上任何自发的氧化还原反应都可以设计成原电池.现使用锌电极、铜电极、橙子(酸性介质)设计如图所示的水果电池.
 .
. 、F
、F .
. .
.