��Ŀ����
10�� �������κ��Է���������ԭ��Ӧ��������Ƴ�ԭ��أ���ʹ��п�缫��ͭ�缫�����ӣ����Խ��ʣ������ͼ��ʾ��ˮ����أ�
�������κ��Է���������ԭ��Ӧ��������Ƴ�ԭ��أ���ʹ��п�缫��ͭ�缫�����ӣ����Խ��ʣ������ͼ��ʾ��ˮ����أ���1���õ�صĸ���������п��Zn��������Ӧʽ��Zn-2e-=Zn2+��
��2���������²���������Ƶ�ˮ����أ���ʹ�����Ʒ�������ƫת��
����ˮ�������ʡ����١����ӵ�
����ˮ�������ӡ����ѵ�
�缫��A��þ����B����Ƭ��C��ͭƬ��D��̼��
����ѡ������ˮ����װˮ����أ��������Ͽ�����AB�������п��ܵĵ缫ѡ���������ӦʽΪ2H++2e-=H2����
����ѡ�����ˮ����װˮ����أ��������Ͽ�����ABD�������п��ܵĵ缫ѡ�������ˮ���ļ��Խ�ǿ����صĸ�����ӦʽΪAl-3e-+4OH-=AlO2-+2H2O��
���� ��1��пΪ����������������п���ӣ�
��2�������ˮ����ظ����Ľ����Դ����������ɣ������������ӵõ��ӷ�����ԭ��Ӧ��
������ɼ��Ե�أ���������Al�������������ܵ�������ʼ��ɣ�
��� �⣺��1�����ý���Zn��ԭ��صĸ���������������Ӧ���缫����ʽΪ���ʴ�Ϊ��п��Zn��Zn-2e-=Zn2+��
��2��������ˮ������У������ܺ��ᷴӦ�������Ͽ�����þ�����������������ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ2H++2e-=H2����
�ʴ�Ϊ��AB��2H++2e-=H2����
������ɼ��Ե�أ���������Al�������������ܵ�������ʼ��ɣ���������������þ��ͭ��̼��������ˮ���ļ��Խ�ǿ����صĸ�����ӦʽΪ
�ʴ�Ϊ��ABD��Al-3e-+4OH-=AlO2-+2H2O��
���� ���⿼����ԭ���ԭ�����������жϼ��缫��Ӧʽ����д��������Һ�е缫���ϵ�ʧ���ӵ����׳̶�ȷ����������ע�ⲻ�ܸ��ݽ����Ļ��ǿ���ж���������Ϊ�״��㣮

��ϰ��ϵ�д�
�����Ŀ
20�����������У����ھƾ�����ֱ�Ӽ��ȵ��ǣ�������
| A�� |  | B�� |  | C�� |  | D�� |  |
1��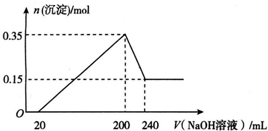 ��һ��������þ���������Ͷ��200 mLϡ�����У�����ȫ���ܽ����������Һ�м���NaOH��Һ�����ɳ��������ʵ���������NaOH��Һ����ı仯��ϵ��ͼ��ʾ��������˵��������ǣ�������
��һ��������þ���������Ͷ��200 mLϡ�����У�����ȫ���ܽ����������Һ�м���NaOH��Һ�����ɳ��������ʵ���������NaOH��Һ����ı仯��ϵ��ͼ��ʾ��������˵��������ǣ�������
 ��һ��������þ���������Ͷ��200 mLϡ�����У�����ȫ���ܽ����������Һ�м���NaOH��Һ�����ɳ��������ʵ���������NaOH��Һ����ı仯��ϵ��ͼ��ʾ��������˵��������ǣ�������
��һ��������þ���������Ͷ��200 mLϡ�����У�����ȫ���ܽ����������Һ�м���NaOH��Һ�����ɳ��������ʵ���������NaOH��Һ����ı仯��ϵ��ͼ��ʾ��������˵��������ǣ�������| A�� | þ������������Ϊ9 g | |
| B�� | ���20 mL NaOH��Һ�����к�����ϡ���� | |
| C�� | ����������Һ�����ʵ���Ũ��Ϊ5 mol•L-1 | |
| D�� | ���ɵ������ڱ�״���µ����Ϊ11.2 L |
15������������ȷ���ǣ�������
| A�� | �����ڿ����е�NaOH��Һ��������ʱ��������� | |
| B�� | 50 mL 12 mol•L-1��Ũ������������MnO2��Ӧ������0.15 mol Cl2 | |
| C�� | �ڳ����£�ŨH2SO4����Cu��Ӧ������Ϊͭ���ۻ� | |
| D�� | CO2ͨ��Ũ��CaCl2��Һ�в�����ɫ���� |
2��ij�Ͻ��������������ʵıȽ������ʾ��������
�����ܿ����úϽ��ʺ��ƣ�������
| ��Ŀ | �۵�/��C | �ܶ�/ ��g•cm-3�� | Ӳ�ȣ���� ʯΪ10�� | ������ ����Ϊ100�� |
| ij�Ͻ� | 2 500 | 3.00 | 7.4 | 2.3 |
| �� | 1 535 | 7.86 | 4.5 | 17 |
| A�� | ���� | B�� | �Ŵ��� | C�� | ¯�� | D�� | �ɻ���� |
19���ִ��������Ŵ���ܳ��õ�Ƽӹ��ɵĹ�ͭɫӲ�����죮ȡӲ����Ʒ������ͼ��ʾ��ʵ�飨ÿһ���Լ������������ɴ˿���֪��Ӳ�������Ϊ��������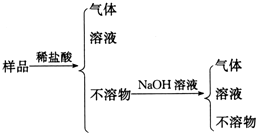

| A�� | Al��Cu��Mg��Si | B�� | Al��Mg��Si��Zn | C�� | Al��Fe��C��Cu | D�� | Al��Si��Zn��Na |

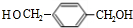 ��������Ӧ������ȡ����Ӧ���Ǣ٢ڣ���������ţ���
��������Ӧ������ȡ����Ӧ���Ǣ٢ڣ���������ţ��� +2NaOH$��_{��}^{H_{2}O}$
+2NaOH$��_{��}^{H_{2}O}$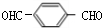 +2H2O��
+2H2O�� ��
��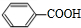 ��
��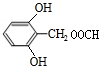 ��
��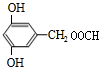 ��д��һ�֣���
��д��һ�֣���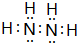 ��
��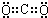 ��
��