17.某实验中需要0.20mol•L-1的Na2CO3溶液950mL,配置该溶液时应选用的容量瓶规格和称取的碳酸钠质量分别是( )
| A. | 950mL、20.14g | B. | 950mL、10.07g | C. | 1000mL、21.20g | D. | 1000mL、10.60g |
16.锌与100mL 18.5mol•L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体甲33.6L(标准状况).将反应后的溶液稀释至1L,测得溶液中c(H+)=0.1mol/L.下列叙述正确的是( )
| A. | 反应中共消耗1.75 mol H2SO4 | B. | 气体甲中SO2与H2的体积比为1:4 | ||
| C. | 反应中共消耗65 g Zn | D. | 反应中共转移3.6 mol电子 |
12.在N2O4(g)?2NO2(g)平衡体系中,增大N2O4的浓度,则NO2和N2O4的物质的量之比,下列叙述正确的是( )
| A. | 一定增大 | B. | 一定减小 | ||
| C. | 一定不变 | D. | 可能减小也可能不变 |
11.在一定条件下,将3mol A和1mol B两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(g).2min后该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol/L,下列判断错误的是( )
| A. | x=1 | |
| B. | 2 min内A的反应速率为0.3 mol/(L•min) | |
| C. | B的转化率为40% | |
| D. | 若混合气体的密度不变,则表明该反应达到平衡状态 |
10.下列物质属于等电子体的一组是( )
| A. | CO2和NO2- | B. | B3H6N3和C6H6 | C. | F-和Mg | D. | H2O和CH4 |
9.清晨松林中的空气格外清新,是因为有极少量的氧气变成了臭氧,反应的化学方程式为:3O2=2O3.太阳初升时,我们还会看到林中有光亮“通路”,下列有关说法正确的是( )
| A. | 上述反应为化合反应 | |
| B. | “通路”是胶体对光产生的丁达尔现象 | |
| C. | 上述反应为氧化还原反应 | |
| D. | 产生的臭氧有毒,会严重影响人体健康 |
8.设阿伏加德罗常数的值为N0,则下列说法正确的是( )
0 153966 153974 153980 153984 153990 153992 153996 154002 154004 154010 154016 154020 154022 154026 154032 154034 154040 154044 154046 154050 154052 154056 154058 154060 154061 154062 154064 154065 154066 154068 154070 154074 154076 154080 154082 154086 154092 154094 154100 154104 154106 154110 154116 154122 154124 154130 154134 154136 154142 154146 154152 154160 203614
| A. | 标准状况下,22.4L乙烯含有的共用电子对数为2N0 | |
| B. | 常温下,含有1 mo1 NaHSO4的溶液中阳离子数为N0 | |
| C. | 通常状况下,1 mo1 NO和0.5 mo1 O2在密闭容器中混合,生成NO2分子数为N0 | |
| D. | 制取漂白粉时,标准状况下22.4 L Cl2参加反应,转移电子数为N0 |


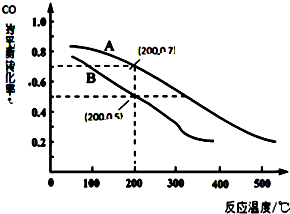 科学家开发出一种“洁净煤技术”,通过向地下煤层“气化炉”中交替鼓入空气和水蒸气的方法,连续产出高热值的煤炭气,其主要成分是CO和H2.“气化炉”中主要反应有:
科学家开发出一种“洁净煤技术”,通过向地下煤层“气化炉”中交替鼓入空气和水蒸气的方法,连续产出高热值的煤炭气,其主要成分是CO和H2.“气化炉”中主要反应有: