13.将32g Cu与150mL一定浓度的HNO3恰好反应,Cu完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L.则下列各项中正确的是( )
| A. | 所用HNO3为浓度为10mol/L | B. | NO的体积为6.72升 | ||
| C. | NO2的体积为3.36升 | D. | 被还原的HNO3为1mol |
12.0.3mol硫化亚铜跟适量硝酸恰好完全反应.反应方程式为:3Cu2S+22HNO3═6Cu(NO3)2+3H2SO4+10NO+8H2O,则反应中未被还原的硝酸的物质的量为( )
| A. | 2.2mol | B. | 1.2mol | C. | 0.6mol | D. | 1.0mol |
11.为鉴别K2CO3和NaHCO3两种白色固体,有4位同学分别设计了不同的方法,其中不可行的是( )
| A. | 将少量的两种白色固体分别加入1 mol/L的盐酸中,看有无气泡产生 | |
| B. | 分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 | |
| C. | 分别取样配成溶液,滴加BaCl2溶液,观察有无白色沉淀 | |
| D. | 分别配成溶液,用铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色 |
10.在6HCl+KClO3═3Cl2↑+KCl+3H2O中,被氧化的氯元素与被还原的氯元素的质量比为( )
| A. | 6:1 | B. | 5:1 | C. | 1:5 | D. | 3:1 |
6.下列叙述正确的是( )
| A. | 稀醋酸中加入少量冰醋酸能增大醋酸的电离程度 | |
| B. | 25℃时,等体积等浓度的盐酸与氨水混合后,溶液pH=7 | |
| C. | 0.1 mol AgCl和0.1mol AgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) | |
| D. | 25℃时,0.1mol•L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱 |
5.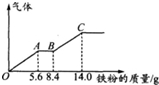 -定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
-定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
 -定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
-定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )| A. | NO,1.5mol/L | B. | H2,1.5mol/L | C. | NO,2.5mol/L | D. | H2,2.5mol/L |
4.为了探究FeS04和Cu(N03)2的混合物中各组分的含量,现设计如下流程.下列叙述中错误的是( ) 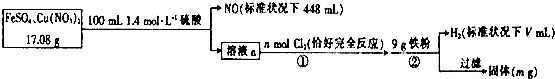
0 153901 153909 153915 153919 153925 153927 153931 153937 153939 153945 153951 153955 153957 153961 153967 153969 153975 153979 153981 153985 153987 153991 153993 153995 153996 153997 153999 154000 154001 154003 154005 154009 154011 154015 154017 154021 154027 154029 154035 154039 154041 154045 154051 154057 154059 154065 154069 154071 154077 154081 154087 154095 203614

| A. | V=2240 | |
| B. | n=0.02 | |
| C. | 原混合物中FeS04的质量分数约为89% | |
| D. | m=0.6 |
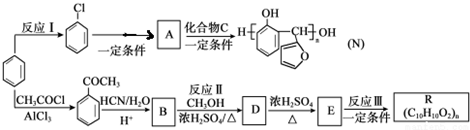
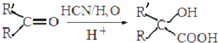
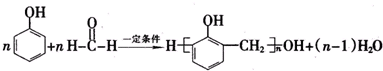
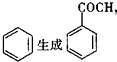 的反应类型是取代反应,D生成E的过程中,浓硫酸的作用是催化剂和脱水剂•
的反应类型是取代反应,D生成E的过程中,浓硫酸的作用是催化剂和脱水剂•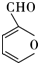
 .
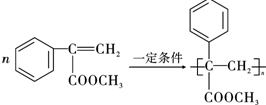
.
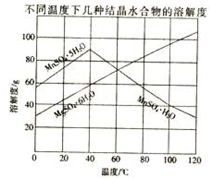 软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4•H2O,反应的化学方程式为:MnO2+SO2=MnSO4
软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4•H2O,反应的化学方程式为:MnO2+SO2=MnSO4