5.在一定条件下,硫酸铵的分解反应为:4(NH4)2SO4=N2↑+6NH3↑+3SO2↑+SO3↑+7H2O,当有nmol电子转移时,下列说法正确的是( )
| A. | 有2nmol(NH4)2SO4分解 | B. | 有$\frac{n}{2}$molS原子被氧化 | ||
| C. | 生成$\frac{n}{6}$mol氧化产物 | D. | 生成7nmolH2O |
4.取一小块金属钠放在燃烧匙中加热,下列实验现象描述正确的是( )
①金属钠先熔化 ②在空气中燃烧,产生黄色火焰 ③燃烧后得白色固体 ④燃烧后生成淡黄色固体物质.
①金属钠先熔化 ②在空气中燃烧,产生黄色火焰 ③燃烧后得白色固体 ④燃烧后生成淡黄色固体物质.
| A. | ①②④ | B. | ①②③ | C. | ①② | D. | ①②③④ |
3.用NA表示阿伏加罗常数的值,下列说法不确的是( )
| A. | 7.1gCl2与足量的氢氧化钠溶液反应生成NaClO转移的电子数为0.1NA | |
| B. | 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去电子数为NA | |
| C. | 常温常压下,32gO2和O3的混合气体所含原子数为2NA | |
| D. | 标准状况下,足量Fe与22.4LCl2反应,转移电子数为3NA |
2.下列有关实验装置进行的相应实验,能达到实验目的是( )
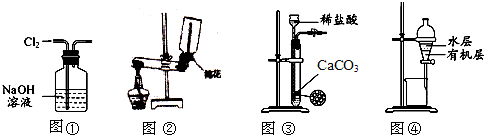

| A. | 用图①所示装置除去Cl2中含有的少量HCl | |
| B. | 用图②所示装置制备并收集O2 | |
| C. | 用图③所示装置制取少量的CO2气体 | |
| D. | 用图④所示装置分离汽油萃取碘水后已分层的有机层和水层 |
1.日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )
| A. | 铜器出现铜绿 | B. | 铁制菜刀生锈 | ||
| C. | 大理石雕像被酸雨腐蚀毁坏 | D. | 铝锅表面生成致密的薄膜 |
20.SF6分子结构中只存在S-F键,是优良的绝缘气体,制备原理如下:S(s)+3F2(g)→SF6(g)△H=?;已知:1mol S(s)转化为气态硫原子吸收能量280kJ,断裂1mol F-F、S-F键需吸收的能量分别为160kJ、330kJ.则△H的值为(单位:kJ?mol-1)( )
| A. | 1780 | B. | 1220 | C. | -1220 | D. | -1780 |
19.下列叙述正确的是( )
| A. | Fe与S混合加热生成FeS2 | |
| B. | NaHCO3的热稳定性大于Na2CO3 | |
| C. | 铁与硝酸反应后溶液中一定有Fe3+存在 | |
| D. | Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
18.下列单质或化合物性质的描述正确的是( )
| A. | NaHSO4水溶液显中性 | |
| B. | NO2溶于水时发生氧化还原反应 | |
| C. | SiO2与酸、碱均不反应 | |
| D. | Fe在足量Cl2中燃烧生成FeCl2和FeCl3 |
17.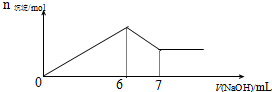 现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L 的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L 的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
 现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L 的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L 的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )| A. | 2:1 | B. | 2:3 | C. | 6:1 | D. | 3:1 |
16.60mL含有0.20mol碳酸钠的溶液和20mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
0 153712 153720 153726 153730 153736 153738 153742 153748 153750 153756 153762 153766 153768 153772 153778 153780 153786 153790 153792 153796 153798 153802 153804 153806 153807 153808 153810 153811 153812 153814 153816 153820 153822 153826 153828 153832 153838 153840 153846 153850 153852 153856 153862 153868 153870 153876 153880 153882 153888 153892 153898 153906 203614
| A. | 10.0 mol/L | B. | 15 mol/L | C. | 1.2 mol/L | D. | 0.9 mol/L |