12.网传云南曲靖市越州镇约5000余吨的重毒化工废料铬渣被非法丢放,毒水被直接排放到南盘江中.
I.某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是C13+,其次是Fe3+、Al3+、Ca2+、Mg2+):
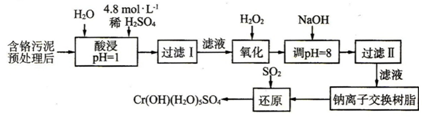
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
(1)实验室用18.4mol/L浓硫酸配制250mL 4.8mol/L硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需250mL容量瓶、胶头滴管.
(2)加入H202的作用是氧化+3价Cr使之转变成+6价Cr(或Cr2O72-),以便于与杂质离子分离.调节溶液的pH=8 是为了除去Fe3+和Al3+离子.
(3)还原过程发生以下反应,请配平:
1Na2Cr2O7+3S02+11H2O═2Cr(OH)(H20)5S04+1Na2S04
(4)钠离子交换树脂的原理为Mn++nNaR═MRn+nNa+,被交换的杂质离子是Ca2+、Mg2+.
Ⅱ.工业废水中常含有一定量的Cr2O72-和Cr042-,它们会对人类及生态系统产生很大损害,必须进行处理.其中一种处理方法为电解法:该法用Fe做电极,电解含Cr2O72-的酸性废水,随着电解进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀.阳极的电极反应式为Fe-2e-=Fe2+.在阴极附近溶液pH升高的原因是2H++2e-=H2 ↑(用电极反应方程式解释).产生的阳极产物在处理废水中铬元素时所起的作用是做还原剂,将+6价的Cr还原为+3价的Cr.
I.某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是C13+,其次是Fe3+、Al3+、Ca2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | ─ | ─ | 4.7 | ─ |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
(2)加入H202的作用是氧化+3价Cr使之转变成+6价Cr(或Cr2O72-),以便于与杂质离子分离.调节溶液的pH=8 是为了除去Fe3+和Al3+离子.
(3)还原过程发生以下反应,请配平:
1Na2Cr2O7+3S02+11H2O═2Cr(OH)(H20)5S04+1Na2S04
(4)钠离子交换树脂的原理为Mn++nNaR═MRn+nNa+,被交换的杂质离子是Ca2+、Mg2+.
Ⅱ.工业废水中常含有一定量的Cr2O72-和Cr042-,它们会对人类及生态系统产生很大损害,必须进行处理.其中一种处理方法为电解法:该法用Fe做电极,电解含Cr2O72-的酸性废水,随着电解进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀.阳极的电极反应式为Fe-2e-=Fe2+.在阴极附近溶液pH升高的原因是2H++2e-=H2 ↑(用电极反应方程式解释).产生的阳极产物在处理废水中铬元素时所起的作用是做还原剂,将+6价的Cr还原为+3价的Cr.
11.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | CO2通过Na2O2使其增重b g时,反应中转移电子数为bNA/44 | |
| B. | 18 g D2O中含有质子的数目为NA | |
| C. | 12 g C3H6 与 16 g C2H4的混合物完全燃烧,可生成CO2分子数为2 NA | |
| D. | 0.1 mol AlCl3完全水解转化为氢氧化铝胶体,生成 0.1 NA个胶粒 |
10.某实验室仅有如下仪器或用具:烧杯、铁架台、铁圈、三脚架、漏斗、分液漏斗、石棉网、酒精灯、玻璃棒、量筒、蒸发皿、圆底烧瓶、火柴.从缺乏仪器的角度看,不能进行的实验项目是( )
| A. | 蒸发 | B. | 萃取 | C. | 液体过滤 | D. | 升华 |
9.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,0.1NA个水分子所占的体积约是2.24 L | |
| B. | 常温常压下,11.2 L CO2中含有11NA个电子 | |
| C. | CH4的摩尔质量和NA个甲烷分子的质量相等 | |
| D. | 常温下,64gSO2气体中含有的原子数为3NA |
8.下列溶液中相应关系正确的是( )
| A. | 0.2 mol•L-1CH3COONa溶液和0.1 mol•L-1HCl溶液等体积混合后:c(CH3COO-)>c(Na+)>c(Cl-)>c(H+)>c(OH-) | |
| B. | pH=3的盐酸和NaOH的混合溶液中:c(Na+)=c(Cl-) | |
| C. | 0.1 mol•L-1NaHCO3 溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| D. | 含SO42-、NH4+、H+、OH-的溶液中可能存在:c(H+)>c(SO42-)>c(NH4+)>c(OH-) |
6.质量分数为15%的硫酸溶液18毫升,密度为1.102g•mL-1,则它的物质的量浓度最接近下列数值中的( )
| A. | 1.685mol•L-1 | B. | 3.370 mol•L-1 | C. | 22.49 mol•L-1 | D. | 11.24 mol•L-1 |
5.下列说法中正确的是( )
| A. | 氯化钠在电流的作用下电离出Na+和Cl- | |
| B. | CaCO3难溶于水,但CaCO3属于强电解质 | |
| C. | 二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质 | |
| D. | 硫酸钠在水中的电离方程式可表示为Na2SO4═2Na++S6++4O2- |
4.物质的体积一定是22.4L的是( )
0 153618 153626 153632 153636 153642 153644 153648 153654 153656 153662 153668 153672 153674 153678 153684 153686 153692 153696 153698 153702 153704 153708 153710 153712 153713 153714 153716 153717 153718 153720 153722 153726 153728 153732 153734 153738 153744 153746 153752 153756 153758 153762 153768 153774 153776 153782 153786 153788 153794 153798 153804 153812 203614
| A. | 1 mol水蒸汽 | B. | 标准状况下1 mol CCl4 | ||
| C. | 标准状况下44 g二氧化碳 | D. | 0℃、202 kPa时2 g氢气 |