题目内容
4.物质的体积一定是22.4L的是( )| A. | 1 mol水蒸汽 | B. | 标准状况下1 mol CCl4 | ||
| C. | 标准状况下44 g二氧化碳 | D. | 0℃、202 kPa时2 g氢气 |
分析 气体摩尔体积指的是在标准状况下,1mol任何气体的体积为22.4L,依据概念进行分析计算.
解答 解:A、1mol水蒸气不是在标准状况下,所以体积不是22.4L,故A错误;
B、标准状况下,四氯化碳是液体,不能利用气体摩尔体积计算,故B错误;
C、标准状况下44g二氧化碳,为1mol,所以标准状况下气体体积为22.4L,故C正确;
D、0℃、202kPa时2g氢气物质的量是1mol,但不是标准状况下,所以体积不一定为22.4L,故D错误;
故选C.
点评 本题考查了气体摩尔体积的概念和应用条件,注意物质的状态必须是气体.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
12.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1.01×105Pa,20℃时48g O3含有的原子数为3NA | |
| B. | 1molNa2O2晶体中阴离子数为2 NA | |
| C. | 标准状况下,相同体积的O2、HCl、H2O含有的分子数相同 | |
| D. | 等质量钠,在足量氧气中加热充分反应比在足量氧气(常温)中充分反应失去的电子多 |
9.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,0.1NA个水分子所占的体积约是2.24 L | |
| B. | 常温常压下,11.2 L CO2中含有11NA个电子 | |
| C. | CH4的摩尔质量和NA个甲烷分子的质量相等 | |
| D. | 常温下,64gSO2气体中含有的原子数为3NA |
13.能正确表示下列反应的离子方程式的是( )
| A. | 将铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O | |
| C. | 将氯化亚铁溶液和氯气反应:Fe2++Cl2═Fe3++2 Cl- | |
| D. | 将铜屑加入含Fe3+的溶液中:2Fe3++Cu═2Fe2++Cu2+ |
14.在下列条件的溶液中,各组离子一定能够大量共存的是( )
| A. | 使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+ | |
| B. | 强酸性溶液中:Na+、K+、NO3-、SiO32- | |
| C. | 可与Al反应放出氢气的溶液中:Na+、Ca2+、Cl-、HCO3- | |
| D. | 使石蕊变蓝的溶液中:Ba2+、Na+、AlO2-、Cl- |
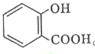 的名称为:2-羟基苯甲酸;在核磁共振氢谱中会出现6组峰;写出其与KHCO3溶液反应的化学方程式:
的名称为:2-羟基苯甲酸;在核磁共振氢谱中会出现6组峰;写出其与KHCO3溶液反应的化学方程式: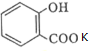 +CO2↑+H2O.
+CO2↑+H2O.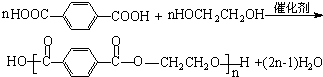 .
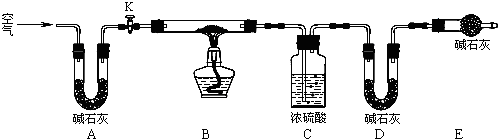
.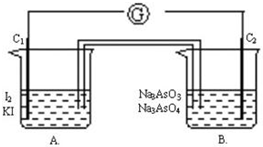 根据可逆反应:AsO43-+2I-+2H+?AsO33-+I2+H2O,设计如下图所示实验装置.
根据可逆反应:AsO43-+2I-+2H+?AsO33-+I2+H2O,设计如下图所示实验装置.