14.下列物质属于两性氧化物的是( )
| A. | CaO | B. | S02 | C. | A1203 | D. | A1(0H)3 |
13. 我国自主研发制造的国产大型客机C919前不久在上海下线,C919的综合监视电子系统是由无锡企业研发制造.电子监视系统的核心部件是其中的电子芯片.制备该电子芯片的材料是( )
我国自主研发制造的国产大型客机C919前不久在上海下线,C919的综合监视电子系统是由无锡企业研发制造.电子监视系统的核心部件是其中的电子芯片.制备该电子芯片的材料是( )
 我国自主研发制造的国产大型客机C919前不久在上海下线,C919的综合监视电子系统是由无锡企业研发制造.电子监视系统的核心部件是其中的电子芯片.制备该电子芯片的材料是( )
我国自主研发制造的国产大型客机C919前不久在上海下线,C919的综合监视电子系统是由无锡企业研发制造.电子监视系统的核心部件是其中的电子芯片.制备该电子芯片的材料是( )| A. | 铝 | B. | 硅 | C. | 碳 | D. | 钢 |
12.研究SO2、NOX、CO等大气污染气体的处理及利用的方法具有重要意义.
(1)火力发电厂的燃煤排烟中含大量的氮氧化物(NOX),可利用甲烷和NOX在一定条件下反应消除其污染.已知:
①N2(g)+O2(g)═2NO(g);△H1=180.5kJ•mol-1
②2NO(g)+O2(g)═2NO2(g);△H2=-113.0kJ•mol-1
③CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H3=-889.5kJ•mol-1
则NO2与CH4转化成N2和H2O(l)的热化学方程式为2NO2(g)+CH4(g)=N2(g)+CO2(g)+2H2O(l)△H=-957kJ•mol-1.
(2)用活性炭还原法也可以处理氮氧化物,有关反应为C(s)+2NO(g)?N2(g)+CO2(g).一定温度下密闭容器中反应有关数据如下表:
①判断该反应达到平衡状态的标志是abd(填字母).
a.v正(NO)=2v逆(N2)
b.N2的浓度保持不变
c.容器中气体的压强不变
d.CO2的体积分数不变
②若平衡后升高温度 ,再次达到平衡测得容器中NO、N2、CO2的浓度值比为5:3:3,则△H<0(填“>”、“=”或“<”).
,再次达到平衡测得容器中NO、N2、CO2的浓度值比为5:3:3,则△H<0(填“>”、“=”或“<”).
(3)利用如图所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2.
①a为电源的正极(填“正极”或“负极”),阳极的电极反应式为SO2+2H2O-2e-=SO42-+4H+.
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO42-生成.该反应中氧化剂与还原剂的物质的量之比为1:2.
(1)火力发电厂的燃煤排烟中含大量的氮氧化物(NOX),可利用甲烷和NOX在一定条件下反应消除其污染.已知:
①N2(g)+O2(g)═2NO(g);△H1=180.5kJ•mol-1
②2NO(g)+O2(g)═2NO2(g);△H2=-113.0kJ•mol-1
③CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H3=-889.5kJ•mol-1
则NO2与CH4转化成N2和H2O(l)的热化学方程式为2NO2(g)+CH4(g)=N2(g)+CO2(g)+2H2O(l)△H=-957kJ•mol-1.
(2)用活性炭还原法也可以处理氮氧化物,有关反应为C(s)+2NO(g)?N2(g)+CO2(g).一定温度下密闭容器中反应有关数据如下表:
| NO | N2 | CO2 | |
| 起始浓度/mol•L-1 | 0.10 | 0 | 0 |
| 平衡浓度/mol•L-1 | 0.04 | 0.03 | 0.03 |
a.v正(NO)=2v逆(N2)
b.N2的浓度保持不变
c.容器中气体的压强不变
d.CO2的体积分数不变
②若平衡后升高温度
 ,再次达到平衡测得容器中NO、N2、CO2的浓度值比为5:3:3,则△H<0(填“>”、“=”或“<”).
,再次达到平衡测得容器中NO、N2、CO2的浓度值比为5:3:3,则△H<0(填“>”、“=”或“<”).(3)利用如图所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2.
①a为电源的正极(填“正极”或“负极”),阳极的电极反应式为SO2+2H2O-2e-=SO42-+4H+.
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO42-生成.该反应中氧化剂与还原剂的物质的量之比为1:2.
9.常温下有体积相同的四种溶液:①pH=3的CH3COOH溶液②pH=3的盐酸③PH=11的氨水④PH=11的NaOH溶液,下列说法正确的是( )
| A. | ①和②混合溶液中:c(H+)不变 | |
| B. | ①和④混合溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | ②和③混合溶液中:溶质只有NH4Cl | |
| D. | ③和④分别用等浓度的盐酸中和,消耗盐酸的体积相同 |
8.下列说法正确的是( )
| A. | 氯碱工业中NaOH的溶液在阳极区产生 | |
| B. | 电解精炼铜时,阳极质量的减小等于阴极质量的增加 | |
| C. | 铁制品表面镀镍时,镀件做阳极 | |
| D. | 电解法制铝的过程中需不断补充阳极材料(石墨电极) |
7.下列关于工业合成氨的叙述正确的是( )
| A. | 合成氨工业温度选择为700K左右,只要是为了提高NH3产率 | |
| B. | 使用催化剂和施加高压,都能提高反应速率,但对化学平衡状态无影响 | |
| C. | 合成氨生产过程中将NH3液化分离,可提高N2、H2的转化率 | |
| D. | 合成氨工业中为了提高氢气的利用率,可适当增加氢气浓度 |
6.某小组为研究原电池原理,设计如图装置,下列叙述正确的是( )
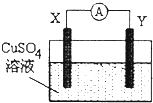

| A. | 若X为Fe,Y为Cu,则铁为正极 | |
| B. | 若X为Ag,Y为Cu,则电流表的指针不发生偏转 | |
| C. | 若X为Cu,Y为Zn,则锌片发生还原反应 | |
| D. | 若X为Fe,Y为C,则碳棒上有红色固体析出 |
5.下列反应的离子方程式书写正确的是( )
0 153450 153458 153464 153468 153474 153476 153480 153486 153488 153494 153500 153504 153506 153510 153516 153518 153524 153528 153530 153534 153536 153540 153542 153544 153545 153546 153548 153549 153550 153552 153554 153558 153560 153564 153566 153570 153576 153578 153584 153588 153590 153594 153600 153606 153608 153614 153618 153620 153626 153630 153636 153644 203614
| A. | 明矾净水:Al3++3H2O∧Al(OH)3+3H+ | |
| B. | 氯气通入水中:Cl2+H2O?2H++ClO-+Cl- | |
| C. | 铜和硝酸银溶液反应:Cu+2Ag+═Cu2++2Ag | |
| D. | 稀硫酸与氢氧化钡溶液反应:Ba2++OH-+H++SO42-═H2O+BaSO4↓ |
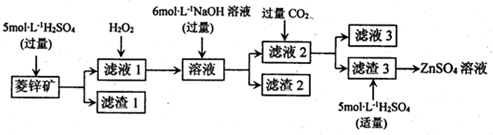
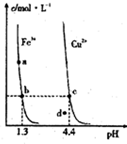 ②常温下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH.金属阳离子浓度的变化如图所示,下列判断正确的是BC.
②常温下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH.金属阳离子浓度的变化如图所示,下列判断正确的是BC.