题目内容
11.由菱锌矿(主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等)制备ZnSO4溶液的流程如图所示: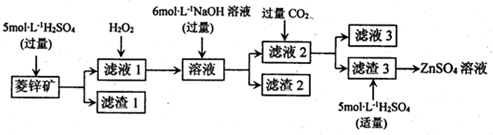
已知:Zn(OH)2与Al(OH)3相似,能溶于过量的NaOH溶液生成Na2[Zn(OH)4].
回答下列问题:
(1)滤渣1主要成分的化学式为SiO2,滤液3中c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)+2c(SO42-).
(2)滤渣1中加入H2O2的目的是将Fe2+氧化成Fe3+以便于转化成沉淀除去,涉及的离子方程式为2H++2Fe2++H2O2=2Fe3++2H2O
(3)已知:KSP[Fe(OH)3]=4.0×10-38,KSP[Cu(OH)2]=2.0×10-20
①常温下,当溶液中加入NaOH溶液使pH=11时Zn(OH)2开始溶解,此时溶液中c(Cu2+)/c(Fe3+)为5.0×1014.Zn(OH)2溶解于NaOH溶液的离子方程式为Zn(OH)2+2OH-=[Zn(OH)4]2-.
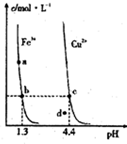 ②常温下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH.金属阳离子浓度的变化如图所示,下列判断正确的是BC.
②常温下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH.金属阳离子浓度的变化如图所示,下列判断正确的是BC.A.加适量氯化铵固体可使溶液由a点变到b点
B.c、d两点代表的溶液中c(H+)与c(OH-)乘积相等
C.Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和
(4)工业上由ZnSO4与BaS溶液混合可制取白色颜料锌钡白(ZnS、BaSO4).在锌钡白中滴加CuSO4溶液振荡后静置,有黑色沉淀产生.原因是ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq)(用离子方程式表示).
分析 由流程可知,菱锌矿的主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等,加硫酸,只有SiO2不反应,经过过滤进行分离,则滤渣1为SiO2,滤液1含有硫酸铜、硫酸亚铁、硫酸锌、剩余的硫酸,加氧化剂将亚铁离子氧化为铁离子,再加过量的NaOH,Zn2+转化ZnO22-,使Cu2+、Fe3+转化为沉淀,通过过滤从溶液中除去,则滤渣2为Fe(OH)3、Cu(OH)2,滤液2中含有Na2ZnO2及过量的NaOH,④通二氧化碳将ZnO22-转化为沉淀,则滤渣3为Zn(OH)2,步骤⑤主要发生氢氧化锌与硫酸的反应,滤液3含有碳酸氢钠,以此解答该题.
解答 解:由流程可知,菱锌矿的主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等,加硫酸,只有SiO2不反应,经过过滤进行分离,则滤渣1为SiO2,滤液1含有硫酸铜、硫酸亚铁、硫酸锌、剩余的硫酸,加氧化剂将亚铁离子氧化为铁离子,再加过量的NaOH,Zn2+转化ZnO22-,使Cu2+、Fe3+转化为沉淀,通过过滤从溶液中除去,则滤渣2为Fe(OH)3、Cu(OH)2,滤液2中含有Na2ZnO2及过量的NaOH,④通二氧化碳将ZnO22-转化为沉淀,则滤渣3为Zn(OH)2,步骤⑤主要发生氢氧化锌与硫酸的反应,滤液3含有碳酸氢钠,
(1)由以上分析可知滤渣1主要成分为SiO2,滤液3含有碳酸氢钠,和硫酸钠,由电荷守恒可知c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)+2c(SO42-),
故答案为:SiO2;c(OH-)+c(HCO3-)+2c(CO32-)+2c(SO42-);
(2)过氧化氢具有强氧化性,可氧化亚铁离子,反应的离子方程式为2H++2Fe2++H2O2=2Fe3++2H2O,将Fe2+氧化成Fe3+以便于转化成沉淀除去,
故答案为:将Fe2+氧化成Fe3+以便于转化成沉淀除去;2H++2Fe2++H2O2=2Fe3++2H2O;
(3)①溶液中加入NaOH溶液使pH=11时,c(Cu2+)=$\frac{2.0×1{0}^{-20}}{(1×1{0}^{-3})^{2}}$=2.0×10-14mol/L,c(Fe3+)=$\frac{4.0×1{0}^{-38}}{(1×1{0}^{-3})^{3}}$mol/L=4.0×10-29mol/L,
则溶液中c(Cu2+)/c(Fe3+)为5.0×1014,
Zn(OH)2与Al(OH)3相似,能溶于过量的NaOH溶液生成Na2[Zn(OH)4],Zn(OH)2溶解于NaOH溶液的离子方程式为Zn(OH)2+2OH-=[Zn(OH)4]2-,
故答案为:5.0×1014;Zn(OH)2+2OH-=[Zn(OH)4]2-;
②A.向溶液中加入NH4Cl固体,铵根离子与氢氧根离子结合生成一水合氨,会导致溶液中的c(OH-)减小,故不能使溶液由a点变到b点,故A错误;
B.只要温度不发生改变,Kw就不变,该题中温度条件不变,c、d两点代表的溶液中c(H+)与c(OH-)乘积相等,故B正确;
C.曲线为沉淀溶解平衡曲线,曲线上的点为平衡点,已知b、c两点分别处在两条的沉淀溶解平衡曲线上,所以两点均代表溶液达到饱和,故C正确,
故答案为:BC;
(4)CuS的溶度积较小,则可转化为CuS黑色沉淀,发生ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq),故答案为:ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq).
点评 本题考查物质制备流程分析判断,为高频考点,侧重于学生的分析、实验和计算能力的考查,把握环节中所得物质成分及除杂试剂、循环利用的物质推断为解答的关键,涉及离子方程式、实验方案的评价等,题目难度中等.

| 时间(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4) | 0.20 | a | 0.10 | c | d | e |
| C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(1)该反应的化学方程式为N2O4?2NO2,表中b>c(填“<”、“=”或“>”).
(2)0~20s内N2O4的平均反应速率为0.003mol/(L•s).
(3)该反应的平衡常数表达式K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$,在80℃时该反应的平衡常数K值为0.54(保留2位小数).
| A. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同 | |
| B. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| C. | 在加热条件下发生的反应均为吸热反应 | |
| D. | 物质发生化学反应时不一定都伴随着能量变化 |
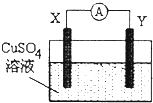
| A. | 若X为Fe,Y为Cu,则铁为正极 | |
| B. | 若X为Ag,Y为Cu,则电流表的指针不发生偏转 | |
| C. | 若X为Cu,Y为Zn,则锌片发生还原反应 | |
| D. | 若X为Fe,Y为C,则碳棒上有红色固体析出 |
| A. | 质子数 | B. | 质量数 | C. | 中子数 | D. | 电子数 |
| A. | 乙烯的结构简式:C2H4 | |
| B. | HCl的电子式: | |
| C. | CH3COOH官能团名称:羟基 | |
| D. | 氨水的电离方程式:NH3•H2O?NH${\;}_{4}^{+}$+OH- |
| A. | 玻璃钢和钢化玻璃成分不同,但都属于复合材料 | |
| B. | Fe(OH)3胶体无色、透明,能发生丁达尔现象 | |
| C. | H2、SO2、Cl2都可用浓硫酸干燥 | |
| D. | SiO2既能和NaOH溶液反应又能和氢氟酸反应,所以是两性氧化物 |
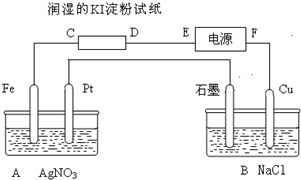 有电解装置如图所示.图中A装置盛1L 2mol/L AgNO3溶液.通电后,润湿的淀粉KI试纸的C端变蓝色,电解一段时间后试回答:
有电解装置如图所示.图中A装置盛1L 2mol/L AgNO3溶液.通电后,润湿的淀粉KI试纸的C端变蓝色,电解一段时间后试回答: