4.传感器可以检测空气中SO2的含量,传感器工作原理如图所示.下列叙述正确的是( )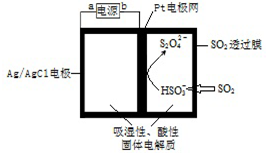

| A. | 阴极发生氧化反应 | |
| B. | 当电路中电子转移为5×10-5mol时,进入传感器的SO2为 1.12 mL | |
| C. | 正极反应式 Ag-e-=Ag+ | |
| D. | b为电源的负极 |
3.锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:
Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是( )
Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是( )
| A. | 电池工作时,锌失去电子,电解液内部OH-向负极移动 | |
| B. | 电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e-═Mn2O3(s)+2OH-(aq) | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
2.在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.
(1)该反应的化学方程式为N2O4?2NO2,表中b>c(填“<”、“=”或“>”).
(2)0~20s内N2O4的平均反应速率为0.003mol/(L•s).
(3)该反应的平衡常数表达式K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$,在80℃时该反应的平衡常数K值为0.54(保留2位小数).
| 时间(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4) | 0.20 | a | 0.10 | c | d | e |
| C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(1)该反应的化学方程式为N2O4?2NO2,表中b>c(填“<”、“=”或“>”).
(2)0~20s内N2O4的平均反应速率为0.003mol/(L•s).
(3)该反应的平衡常数表达式K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$,在80℃时该反应的平衡常数K值为0.54(保留2位小数).
1.PbO2、KMnO4、C12、FeC13、CuC12的氧化性依次减弱.下列反应在水溶液中不可能发生的是( )
| A. | Cu+2Fe3+═Cu2++2Fe2+ | |
| B. | 1OCI-+2MnO4一+16H+═2Mn2++5Cl2↑+8H2O | |
| C. | 2Cu+C12$\frac{\underline{\;点燃\;}}{\;}$2CuC12 | |
| D. | 5Pb2++2MnO4一+2H2O═5PbO2+2Mn2++4H+ |
20.a为乙二胺四乙酸(EDTA),易与金属离子形成螯合物.b为EDTA与Ca2+形成的螯合物.下列叙述正确的是( )
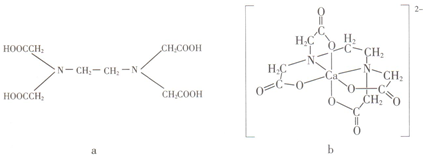

| A. | a和b中的N原子均为sp3杂化 | B. | b中Ca2+的配位数为4 | ||
| C. | b含有分子内氢键 | D. | b含有共价键、离子键和配位键 |
19.如图三条曲线表示C、Si和P元素的四级电离能变化趋势.下列说法正确的是( )
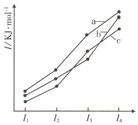

| A. | 电负性:c>b>a | B. | 最简单氢化物的稳定性:c>a>b | ||
| C. | I5:a>c>b | D. | 最简单氢化物的沸点:a>b>c |
18.铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法不正确的是( )
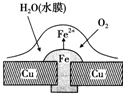

| A. | 正极的电极反应为:2H++2e-═H2↑ | |
| B. | 此过程中还涉及反应:4Fe(OH)2+2H2O+O2═4Fe(OH)3 | |
| C. | 此过程中铜并不被腐蚀 | |
| D. | 此过程中电子从Fe移向Cu |
17.已知0.1mol/L的醋酸溶液中存在如下电离平衡CH3COOH?CH3COO-+H+,并测得其在t℃时Ka=b,下列说法中正确的是( )
| A. | 增大c(CH3COOH),b增大 | B. | 加水稀释,b减小 | ||
| C. | b的大小只与温度有关 | D. | 以上说法均不对 |
16.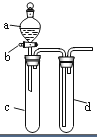 某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.
某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是检查装置的气密性.
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2mL浓硝酸,c中反应的化学方程式是Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是丙.
(4)该小组还用上述装置进行实验证明酸性:HCl>H2CO3>H2SiO3,则分液漏斗a中加入的试剂是稀盐酸,c中加入的试剂是大理石(或Na2CO3固体),d中加入的试剂是Na2SiO3溶液;实验现象为c中有气泡产生,d中生成白色胶状物质(或白色沉淀).但此实验存在不足之处,改进的措施是在c、d之间连接一个盛有饱和NaHCO3溶液的洗气瓶.
 某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.
某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是检查装置的气密性.
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2mL浓硝酸,c中反应的化学方程式是Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
| 方案 | 反应物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明酸性:HCl>H2CO3>H2SiO3,则分液漏斗a中加入的试剂是稀盐酸,c中加入的试剂是大理石(或Na2CO3固体),d中加入的试剂是Na2SiO3溶液;实验现象为c中有气泡产生,d中生成白色胶状物质(或白色沉淀).但此实验存在不足之处,改进的措施是在c、d之间连接一个盛有饱和NaHCO3溶液的洗气瓶.
15.将铜片投入到稀硫酸中,铜片不溶,加入下列试剂后,可使铜片溶解的是( )
0 153447 153455 153461 153465 153471 153473 153477 153483 153485 153491 153497 153501 153503 153507 153513 153515 153521 153525 153527 153531 153533 153537 153539 153541 153542 153543 153545 153546 153547 153549 153551 153555 153557 153561 153563 153567 153573 153575 153581 153585 153587 153591 153597 153603 153605 153611 153615 153617 153623 153627 153633 153641 203614
| A. | 稀盐酸 | B. | Na2SO4晶体 | C. | KNO3晶体 | D. | FeCl3晶体 |