20.下列过程中不放出热量的是( )
| A. | 碳酸钠固体中加少量水 | B. | 碳酸氢钠固体中加少量水 | ||
| C. | 钠与水的反应 | D. | 过氧化钠与水反应 |
19.下列仪器中萃取能用到的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
18.下列除杂(括号内为杂质)使用的主要实验方法正确的是( )
| A. | NaCl溶液(CaCO3):加热 | B. | NaHCO3溶液(Na2CO3):加热 | ||
| C. | H2O(NaCl):蒸馏 | D. | 苯(水):萃取 |
17.下列化学品对应的标志正确的是( )
| A. |  天然气 天然气 | B. |  汽油 汽油 | C. |  浓硫酸 浓硫酸 | D. |  高锰酸钾 高锰酸钾 |
16.这几年的北京经常遭遇“四面霾伏”,这种情况的发生的主要原因( )
| A. | 空气中的二氧化硫超标 | B. | 空气中的氮氧化物超标 | ||
| C. | 空气中可吸入颗粒物超标 | D. | 空气中的二氧化碳超标 |
15. 钠及其化合物在生产和生活中有广泛的应用.完成下列计算:
钠及其化合物在生产和生活中有广泛的应用.完成下列计算:
(1)钠铝合金可作核反应堆的载热介质.取1.46g的钠铝合金放入水中,合金全部溶解,放出1.12L氢气(标准状况),则该钠铝合金的化学式为Na2Al.
(2)NaCN是一种剧毒的化工原料,可用双氧水处理含NaCN的废液,发生反应的方程式为:NaCN+H2O2+H2O=NaHCO3+NH3.若处理含NaCN 4.90g的废液,需用15%的H2O221.65mL.(已知15% H2O2的密度是1.047g/mL)(保留2位小数)
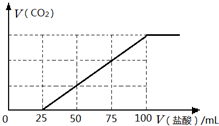
(3)向100mL NaOH溶液中通入一定量的CO2气体,充分反应后得到溶液A,再向A中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.试计算溶液A的溶质成份及其物质的量.
(4)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失.
上述实验①②③所用氢氧化钠均不含杂质,且实验数据可靠.通过计算,分析和比较上表3组数据,给出结论.
0 153376 153384 153390 153394 153400 153402 153406 153412 153414 153420 153426 153430 153432 153436 153442 153444 153450 153454 153456 153460 153462 153466 153468 153470 153471 153472 153474 153475 153476 153478 153480 153484 153486 153490 153492 153496 153502 153504 153510 153514 153516 153520 153526 153532 153534 153540 153544 153546 153552 153556 153562 153570 203614
 钠及其化合物在生产和生活中有广泛的应用.完成下列计算:
钠及其化合物在生产和生活中有广泛的应用.完成下列计算:(1)钠铝合金可作核反应堆的载热介质.取1.46g的钠铝合金放入水中,合金全部溶解,放出1.12L氢气(标准状况),则该钠铝合金的化学式为Na2Al.
(2)NaCN是一种剧毒的化工原料,可用双氧水处理含NaCN的废液,发生反应的方程式为:NaCN+H2O2+H2O=NaHCO3+NH3.若处理含NaCN 4.90g的废液,需用15%的H2O221.65mL.(已知15% H2O2的密度是1.047g/mL)(保留2位小数)
(3)向100mL NaOH溶液中通入一定量的CO2气体,充分反应后得到溶液A,再向A中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.试计算溶液A的溶质成份及其物质的量.
(4)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失.
| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
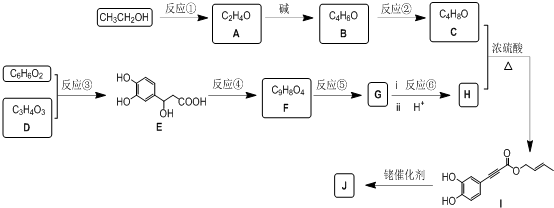
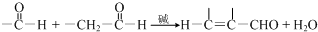
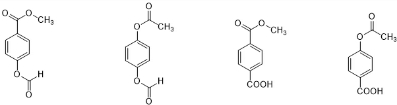 任意一种.
任意一种.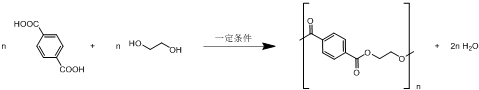 .
. .
.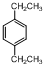 .
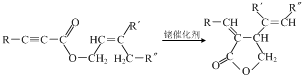
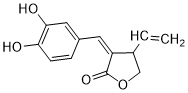
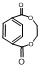
.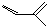 ,两分子该单体发生“Diels-Alder反应”,写出两种不同结构的产物
,两分子该单体发生“Diels-Alder反应”,写出两种不同结构的产物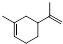 、
、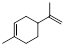 .
.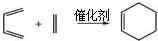
 .
.