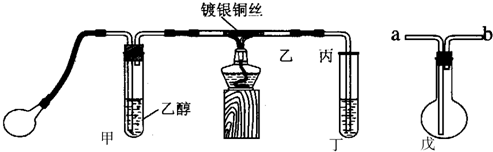
11.利用下列装置(部分仪器已省略),能顺利完成对应实验的是( )
| A. | 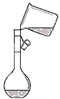 是向容量瓶转移溶液 | |
| B. | 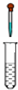 制取氢氧化亚铁 | |
| C. | 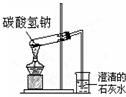 是碳酸氢钠受热分解 | |
| D. | 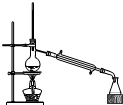 分离四氯化碳(沸点76.75℃)和甲苯(沸点为110.6℃)的混合物 |
9.氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质.下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A. | 使新鲜的红玫瑰花褪色(HCl) | B. | 新制氯水呈浅黄绿色(Cl2) | ||
| C. | 加入小苏打固体,有气泡产生(H+) | D. | 滴加AgNO3溶液生成白色沉淀(Cl-) |
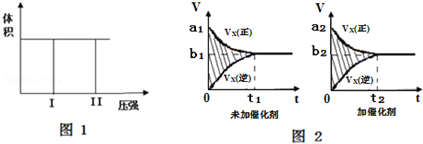
8.为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )
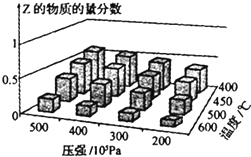

| A. | 在恒温恒压条件下,向已达到平衡的体系中加入少量Z,达新平衡时,Z的物质的量分数增大 | |
| B. | 升高温度,正、逆反应速率都增大,平衡常数增大 | |
| C. | △H>0 m+n>c | |
| D. | 温度不变,减小压强,平衡逆向移动,达新平衡时,A的浓度比原平衡减小 |
6.下列说法正确的是( )
| A. | 乙烯的结构简式为CH2=CH2,可以用作果实催熟剂 | |
| B. | 淀粉和纤维素分子式均可表示成(C6H10O5)n,它们互为同分异构体 | |
| C. | 己烷和苯可以用酸性高锰酸钾溶液来鉴别 | |
| D. | 糖类、油脂、蛋白质都可以发生水解反应 |
5.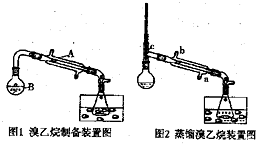 已知乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如下表所示:
已知乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如下表所示:
某研究性学习小组的同学将乙醇、80%的硫酸、NaBr固体按一定比例混合后(总体积约140mL)置于图1
的反应容器B中后进行加热(两个装置中的加热、固定装置及沸石均省略).
(1)①仪器A的名称是:冷凝管;②容器B的容积是:c,
a.150mL b.200mL c.250mL
(2)两个水槽中的液体均是冰水,使用冰水的目的是降温,减少溴乙烷的挥发.
(3)HBr与乙醇反应生成目标产物的化学方程式HBr+C2H5OH$\stackrel{加热}{→}$C2H5Br+H2O.
(4)图1中收集到的产品中含有一定量的杂质Br2.为除去该杂质,可先向混合液中加入适量的(从下面所给试剂中选取)b,然后再进行分液操作即可.
a.四氯化碳 b.碳酸钠稀溶液 c.无水CaCl2 d.无水MgSO4
(5)经过(4)处理后的目标产物中还含有少量的水等杂质,可通过向产品中加入一定量的cd(从上面的a~d中选取),充分作用后,过滤,将滤液使用图2中的装置进行提纯,冷却水应从a口(填a或b)进入.
(6)若实验中使用的无水乙醇的体积是46mL,蒸馏后得到的纯溴乙烷的体积是50rnL,则溴乙烷的产率为80%.
 已知乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如下表所示:
已知乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如下表所示:| 溶解性(本身均做溶剂) | 沸点(℃) | 密度(g/mL) | |
| 水混溶,易溶于有机溶剂 | 78.5 | 0.8 | |
| 难溶于水,易溶于有机溶剂 | 38.4 | 1.4 |
的反应容器B中后进行加热(两个装置中的加热、固定装置及沸石均省略).
(1)①仪器A的名称是:冷凝管;②容器B的容积是:c,
a.150mL b.200mL c.250mL
(2)两个水槽中的液体均是冰水,使用冰水的目的是降温,减少溴乙烷的挥发.
(3)HBr与乙醇反应生成目标产物的化学方程式HBr+C2H5OH$\stackrel{加热}{→}$C2H5Br+H2O.
(4)图1中收集到的产品中含有一定量的杂质Br2.为除去该杂质,可先向混合液中加入适量的(从下面所给试剂中选取)b,然后再进行分液操作即可.
a.四氯化碳 b.碳酸钠稀溶液 c.无水CaCl2 d.无水MgSO4
(5)经过(4)处理后的目标产物中还含有少量的水等杂质,可通过向产品中加入一定量的cd(从上面的a~d中选取),充分作用后,过滤,将滤液使用图2中的装置进行提纯,冷却水应从a口(填a或b)进入.
(6)若实验中使用的无水乙醇的体积是46mL,蒸馏后得到的纯溴乙烷的体积是50rnL,则溴乙烷的产率为80%.
4. 在温度T1和T2下,X2(g)和H2(g)反应生成HX(g)的平衡常数K如下表:
在温度T1和T2下,X2(g)和H2(g)反应生成HX(g)的平衡常数K如下表:
(1)仅依据K的变化可推断出随着卤素原子核电荷数的增加cd(填字母)
a.HX的还原性逐渐减弱 b.X2与H2反应的剧烈程度逐渐减弱
c.HX的稳定性逐渐减弱 d.在相同条件下,X2的平衡转化率逐渐降低
(2)在容积为3L的密闭容器中,由I2(g)和H2(g)合成HI(g),在其他条件不变的情况下,研究温度对反应的影响,HI的物质的量的变化情况如图所示:
①温度为T1时,在0~tAmin内,H2的消耗速率v (H2)=$\frac{{n}_{A}}{6{t}_{A}}$mol/(L•min)
②分析图象,下列说法正确的是a、b(填序号)
a.平衡常数K随温度的升高而变小 b.正反应为放热反应
c.只有当反应进行到A点或B点所示状态时,容器内气体密度才不再发生变化
(3)已知氢氟酸(HF)是弱酸,加水稀释0.1mol•L-1HF溶液,下列各量中增大的是D(填序号)
a.c(H+) b.HF的电离常数 c.c(F-)/c(H+) d.c(H+)/c(HF)
(4)向盛有10滴0.1mol•L-1AgNO3溶液的试管中滴加0.1mol•L-1 NaCl溶液至不再有白色沉淀生成,向其中再滴加0.1mol•L-1KI溶液,出现了黄色沉淀.请简要解释此现象的原因:AgI溶解度比AgCl溶解度小,使AgCl(s)?Ag+(aq)+Cl-(aq)体系中c(Ag+)减小,使平衡向右移动.
 在温度T1和T2下,X2(g)和H2(g)反应生成HX(g)的平衡常数K如下表:
在温度T1和T2下,X2(g)和H2(g)反应生成HX(g)的平衡常数K如下表:| 化学方程式 | K(t1) | K(t2) |
| F2+H2?2HF | 1.8×1036 | 1.9×1032 |
| Cl2+H2?2HCl | 9.7×1012 | 4.2×1011 |
| Br2+H2?2HBr | 5.6×107 | 9.3×106 |
| I2+H2?2HI | 43 | 34 |
a.HX的还原性逐渐减弱 b.X2与H2反应的剧烈程度逐渐减弱
c.HX的稳定性逐渐减弱 d.在相同条件下,X2的平衡转化率逐渐降低
(2)在容积为3L的密闭容器中,由I2(g)和H2(g)合成HI(g),在其他条件不变的情况下,研究温度对反应的影响,HI的物质的量的变化情况如图所示:
①温度为T1时,在0~tAmin内,H2的消耗速率v (H2)=$\frac{{n}_{A}}{6{t}_{A}}$mol/(L•min)
②分析图象,下列说法正确的是a、b(填序号)
a.平衡常数K随温度的升高而变小 b.正反应为放热反应
c.只有当反应进行到A点或B点所示状态时,容器内气体密度才不再发生变化
(3)已知氢氟酸(HF)是弱酸,加水稀释0.1mol•L-1HF溶液,下列各量中增大的是D(填序号)
a.c(H+) b.HF的电离常数 c.c(F-)/c(H+) d.c(H+)/c(HF)
(4)向盛有10滴0.1mol•L-1AgNO3溶液的试管中滴加0.1mol•L-1 NaCl溶液至不再有白色沉淀生成,向其中再滴加0.1mol•L-1KI溶液,出现了黄色沉淀.请简要解释此现象的原因:AgI溶解度比AgCl溶解度小,使AgCl(s)?Ag+(aq)+Cl-(aq)体系中c(Ag+)减小,使平衡向右移动.
3.在一密闭容器中,反应aA(g)?bB(g)达到平衡后,保持温度不变,将容器体积扩大到原体积的2倍,达到新的平衡后,B的浓度是原来的0.6倍,则下列叙述不正确的是( )
0 153300 153308 153314 153318 153324 153326 153330 153336 153338 153344 153350 153354 153356 153360 153366 153368 153374 153378 153380 153384 153386 153390 153392 153394 153395 153396 153398 153399 153400 153402 153404 153408 153410 153414 153416 153420 153426 153428 153434 153438 153440 153444 153450 153456 153458 153464 153468 153470 153476 153480 153486 153494 203614
| A. | 平衡向正反应方向移动 | B. | 物质A的转化率增大 | ||
| C. | 物质B的质量分数增加 | D. | a>b |
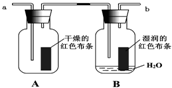 为了探究“红色布条褪色的原因与次氯酸有关而跟氯气无关”.某学生设计了如图装置进行实验.请回答:
为了探究“红色布条褪色的原因与次氯酸有关而跟氯气无关”.某学生设计了如图装置进行实验.请回答: