题目内容
8.为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )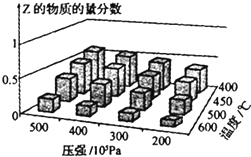
| A. | 在恒温恒压条件下,向已达到平衡的体系中加入少量Z,达新平衡时,Z的物质的量分数增大 | |
| B. | 升高温度,正、逆反应速率都增大,平衡常数增大 | |
| C. | △H>0 m+n>c | |
| D. | 温度不变,减小压强,平衡逆向移动,达新平衡时,A的浓度比原平衡减小 |
分析 由图象可知,降低温度,Z的物质的量分数增大,说明降低温度平衡向正反应方向移动,所以正反应是放热的,则△H<0,
降低压强,Z的物质的量分数减小,说明压强减小,平衡向着逆反应方向移动,减小压强,化学平衡是向着气体系数和增加的方向进行的,所以有m+n>c,由此分析解答.
解答 解:由图象可知,降低温度,Z的物质的量分数增大,说明降低温度平衡向正反应方向移动,所以正反应是放热的,则△H<0,
降低压强,Z的物质的量分数减小,说明压强减小,平衡向着逆反应方向移动,减小压强,化学平衡是向着气体系数和增加的方向进行的,所以有m+n>c,
A、在恒温恒压条件下,向已达到平衡的体系中加入少量Z,为保持压强不变体积增大,最后达到相同平衡状态,但Z的含量不变,故A错误;
B、升高温度正逆反应速率都加快,但因正反应是放热反应,所以平衡常数减小,故B错误;
C、正反应是放热的,则△H<0,减小压强,化学平衡是向着气体系数和增加的方向进行的,所以有m+n>c,故C错误;
D、由C知,△H<0 m+n>c,温度不变,减小压强,体积增大,平衡逆向移动,达新平衡时,体积改变其主要作用.所以A的浓度比原平衡减小,故D正确;
故选D.
点评 本题考查温度、压强等外界条件对平衡移动的影响,题目难度中等,解答本题的关键是能正确分析图象曲线的变化趋势.

练习册系列答案
相关题目
20.下列说法正确的是( )
| A. | 秸秆、毛发及塑料完全燃烧都只生成二氧化碳和水 | |
| B. | 纤维素、油脂、蛋白质都能发生水解反应,都属于天然有机高分子化合物 | |
| C. | 苯和乙烯都能使溴水褪色,均与溴发生加成反应 | |
| D. | 蛋白质遇饱和硫酸铵溶液产生的沉淀能重新溶于水 |
1.根据如图提供的信息,下列所得结论不正确的是( )
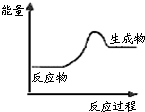

| A. | 该反应为放热反应 | |
| B. | 该反应一定有能量转化成了化学能 | |
| C. | 反应物比生成物稳定 | |
| D. | 因为反应物的总能量低于生成物的总能量,所以该反应需要加热才能发生 |
16.下列叙述中,错误的是( )
| A. | 甲苯与氯气在光照下反应主要生成2,4-二氯甲苯 | |
| B. | 苯和浓硝酸、浓硫酸共热并保持50-60℃反应生成硝基苯 | |
| C. | 甲苯在合适条件下催化加氢可生成甲基环己烷 | |
| D. | 乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 |
3.在一密闭容器中,反应aA(g)?bB(g)达到平衡后,保持温度不变,将容器体积扩大到原体积的2倍,达到新的平衡后,B的浓度是原来的0.6倍,则下列叙述不正确的是( )
| A. | 平衡向正反应方向移动 | B. | 物质A的转化率增大 | ||
| C. | 物质B的质量分数增加 | D. | a>b |
13.除去下列物质中少量杂质的方法正确的是( )
| A. | 除去CO2中混有的HCl:用饱和碳酸钠溶液洗气 | |
| B. | 除去Cu粉中混有的CuO:加适量稀硝酸后,过滤 | |
| C. | 除去Al2O3中混有的SiO2:加NaOH溶液,过滤 | |
| D. | 除去Fe2O3中混有少量的Fe(OH)3:加热灼烧 |
20.化学与能源开发、环境保护、资源利用、食品安全等密切相关,下列说法正确的是( )
| A. | 自来水生产中应尽量用氯气消毒 | |
| B. | 充分利用地沟油提炼食用油,提高原料利用率 | |
| C. | 添加硫酸铁制“铁强化酱油”,添加碘酸钾制加碘盐 | |
| D. | 高纯硅及其氧化物在太阳能电池及信息高速传输中有重要应用 |
18.下列关于物质应用和组成的说法正确的是( )
| A. | 浓硫酸可用于干燥Cl2和NH3 | |
| B. | 正常雨水的pH小于7 | |
| C. | CCl4可用于萃取碘水中的碘,但酒精不可以用于萃取碘水中的碘 | |
| D. | Si可用于制造光导纤维 |

 ,其中反应(1)的条件是氢氧化钠水溶液、加热;
,其中反应(1)的条件是氢氧化钠水溶液、加热; ;
; 也能与化合物Ⅱ发生类似反应①的反应,除CH3COOH外,另一种有机产物的结构简式为
也能与化合物Ⅱ发生类似反应①的反应,除CH3COOH外,另一种有机产物的结构简式为 .
.