13.若NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A. | 标准状况下,22.4 L H2和Cl2的混合气体中含有的分子数为2NA | |
| B. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| C. | NA个氧气分子与NA个氖气分子的质量比是8:5 | |
| D. | 标准状况下,11.2 L CO2与常温常压下8.5 g NH3所含分子数相等 |
12.下列物质的分类与对应化学式正确的组是( )
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | KOH | CH3COOH | Na2CO3 | Al2O3 | SO2 |
| B | NaOH | HCl | NaHCO3 | Na2O | CO |
| C | Ba(OH)2 | H2SO4 | CaCl2 | MgO | CO2 |
| D | Ca(OH)2 | HNO3 | NaCl | Na2O2 | SO3 |
| A. | A | B. | B | C. | C | D. | D |
11.下列反应中的氨与反应4NH3+5O2═4NO+6H2O中的氨作用相同的是( )
| A. | NaOH+NH4Cl═NaCl+NH3↑+H2O | B. | 2NH3+3CuO═3Cu+N2+3H2O | ||
| C. | 2Na+2NH3═2NaNH2+H2↑ | D. | NH3+CO2+H2O═NH4HCO3 |
10.下列说法正确的是( )
| A. | 将(CH3)3CCH2Cl与氢氧化钾的乙醇溶液加热一段时间后冷却,再滴加硝酸酸化的硝酸银溶液,可观察到有白色沉淀产生 | |
| B. | 新制氢氧化铜悬浊液可检验失去标签的乙醛、乙酸、乙酸乙酯(必要时可加热) | |
| C. | 在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀 | |
| D. | 向淀粉溶液中加稀硫酸,加热几分钟,冷却后加入新制氢氧化铜悬浊液,若加热后未见砖红色沉淀生成,说明淀粉未开始水解 |
9.某溶液中可能含有大量的下列离子:NH4+、K+、A1O2-、CO32-、SO32-、C1-中的若干种.现设计并完成了如下实验: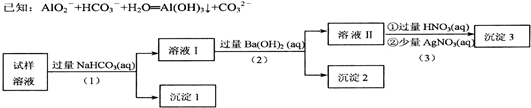
根据以上的实验操作与现象,得出的如下结论中正确的是( )

根据以上的实验操作与现象,得出的如下结论中正确的是( )
| A. | 试样溶液中若(1)加入的是稍过量的FeCl3溶液,则沉淀1物质的成分不变 | |
| B. | 试样溶液中肯定存在阴离子A1O2-、C1-,阳离子NH4+、K+至少存在1种 | |
| C. | 上述沉淀2放置在干燥空气中一段时间后,称量质量没有变化,可判断试样中无SO32- | |
| D. | 实验中,如果将操作(1)与(3)所加的试剂互换,过程中的实验现象仍会完全相同 |
8.Li-Al/FeS电池是一种正在开发的车载电池,该电池正极的反应式为:2Li++FeS+2e-=Li2S+Fe 有关该电池的下列说法中,错误的是( )
| A. | Li-Al在电池中作为负极材料,电极反应式:Li-e-=Li+ | |
| B. | 该电池的电池反应式为:2Li+FeS=Li2S+Fe | |
| C. | 充电时,阴极发生的电极反应式为:Li2S+Fe-2e-═2Li++FeS | |
| D. | 放电时,Li+向正极迁移 |
6.反应2NO(g)+2H2(g)═N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,该反应的速率表达式为v=k•cm(NO)•cn(H2)(k、m、n待测),其反应包含下下列两步:
①2NO+H2═N2+H2O2(慢)
②H2O2+H2═2H2O(快)
T℃时测得有关实验数据如下:
下列说法错误的是( )
①2NO+H2═N2+H2O2(慢)
②H2O2+H2═2H2O(快)
T℃时测得有关实验数据如下:
| 序号 | c(NO)/mol•L-1 | c(H2)/mol•L-1 | 速率/mol•L-1•min-1 |
| Ⅰ | 0.0060 | 0.0010 | 1.8×10-4 |
| Ⅱ | 0.0060 | 0.0020 | 3.6×10-4 |
| Ⅲ | 0.0010 | 0.0060 | 3.0×10-5 |
| Ⅳ | 0.0020 | 0.0060 | 1.2×10-4 |
| A. | 整个反应速度由第①步反应决定 | |
| B. | 正反应的活化能一定是①<② | |
| C. | 该反应速率表达式:v=5000c2(NO)•c(H2) | |
| D. | 该反应的热化学方程式为2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=-664kJ•mol-1 |
5.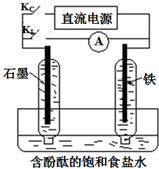 某研究性学习小组设计如下微型实验装置.实验时,先断开KL,闭合KC,两极均有气泡产生;一段时间后,断开KC,闭合KL,发现电流计A指针偏转.下列有关说法正确的是( )
某研究性学习小组设计如下微型实验装置.实验时,先断开KL,闭合KC,两极均有气泡产生;一段时间后,断开KC,闭合KL,发现电流计A指针偏转.下列有关说法正确的是( )
 某研究性学习小组设计如下微型实验装置.实验时,先断开KL,闭合KC,两极均有气泡产生;一段时间后,断开KC,闭合KL,发现电流计A指针偏转.下列有关说法正确的是( )
某研究性学习小组设计如下微型实验装置.实验时,先断开KL,闭合KC,两极均有气泡产生;一段时间后,断开KC,闭合KL,发现电流计A指针偏转.下列有关说法正确的是( )| A. | 断开KL,闭合KC时,铁作阴极,总反应方程式为2H2O=2H2↑+O2↑ | |
| B. | 断开KL,闭合KC时,石墨电极附近溶液变红 | |
| C. | 断开KC,闭合KL时,石墨作正极,发生还原反应Cl2+2e-=2Cl- | |
| D. | 断开KC,闭合KL时,铁作负极,发生铁的吸氧腐蚀反应 |
4.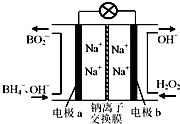 以硼氢化合物NaBH4(强电解质,B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )
以硼氢化合物NaBH4(强电解质,B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )
0 153294 153302 153308 153312 153318 153320 153324 153330 153332 153338 153344 153348 153350 153354 153360 153362 153368 153372 153374 153378 153380 153384 153386 153388 153389 153390 153392 153393 153394 153396 153398 153402 153404 153408 153410 153414 153420 153422 153428 153432 153434 153438 153444 153450 153452 153458 153462 153464 153470 153474 153480 153488 203614
 以硼氢化合物NaBH4(强电解质,B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )
以硼氢化合物NaBH4(强电解质,B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )| A. | 电极a采用MnO2,MnO2既作电极材料又有催化作用 | |
| B. | 电池放电时Na+从a极区移向b极区 | |
| C. | 每消耗3mol H2O2,转移的电子为3mol | |
| D. | 该电池的负极反应为:BH4-+8OH--8e-═BO2-+6H2O |