题目内容
6.反应2NO(g)+2H2(g)═N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,该反应的速率表达式为v=k•cm(NO)•cn(H2)(k、m、n待测),其反应包含下下列两步:①2NO+H2═N2+H2O2(慢)
②H2O2+H2═2H2O(快)
T℃时测得有关实验数据如下:
| 序号 | c(NO)/mol•L-1 | c(H2)/mol•L-1 | 速率/mol•L-1•min-1 |
| Ⅰ | 0.0060 | 0.0010 | 1.8×10-4 |
| Ⅱ | 0.0060 | 0.0020 | 3.6×10-4 |
| Ⅲ | 0.0010 | 0.0060 | 3.0×10-5 |
| Ⅳ | 0.0020 | 0.0060 | 1.2×10-4 |
| A. | 整个反应速度由第①步反应决定 | |
| B. | 正反应的活化能一定是①<② | |
| C. | 该反应速率表达式:v=5000c2(NO)•c(H2) | |
| D. | 该反应的热化学方程式为2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=-664kJ•mol-1 |
分析 A.依据反应过程中的两步反应可知,反应慢的决定整个反应速率;
B.反应①难以进行,说明反应的活化能高;
C.比较图表数据ⅠⅡ数据NO浓度不变,氢气浓度增大一倍,反应速率增大一倍,ⅢⅣ数据分析,H2浓度不变,NO浓度增大一倍,反应速率增大到4倍,据此得到速率方程,代入数值计算得到K分析判断方程正误;
D.反应2NO(g)+2H2(g)═N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,生成28gN2放热664KJ,结合热化学方程式书写分析判断,标注物质聚集状态和对应反应的焓变;
解答 解:A.①2NO+H2═N2+H2O2(慢),②H2O2+H2═2H2O(快),反应历程中反应慢的决定反应速率,整个反应速度由第①步反应决定,故A正确;
B.反应①难以进行,说明反应的活化能高,正反应的活化能一定是①>②,故B错误;
C.比较图表数据ⅠⅡ数据NO浓度不变,氢气浓度增大一倍,反应速率增大一倍,ⅢⅣ数据分析,H2浓度不变,NO浓度增大一倍,反应速率增大到4倍,据此得到速率方程,v=Kc2(NO)•c(H2),依据Ⅰ中数据计算K=5000,则速率方程v=5000c2(NO)•c(H2),故C正确;
D.反应2NO(g)+2H2(g)═N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,生成28gN2放热664KJ,热化学方程式为:2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=-664kJ•mol-1,故D正确;
故选B.
点评 本题考查了化学反应能量变化分析,热化学方程式书写,主要是催化剂作用,速率方程的推导和计算应用,题目难度中等.

练习册系列答案
相关题目
16.下列反应的离子方程式,正确的是( )
| A. | Fe溶于稀盐酸:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 用小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O | |
| C. | 用FeCl3溶液腐蚀印刷电路板上铜箔:Fe3++Cu═Fe2++Cu2+ | |
| D. | 铝与浓氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
14.下列说法不正确的是( )
| A. | 胶体一定是混合物 | |
| B. | 丁达尔效应可用于鉴别胶体和溶液 | |
| C. | 明矾溶于水可产生具有吸附性的胶体粒子,常用于净化自来水 | |
| D. | PM2.5是指大气中直径小于或等于2.5微米(2.5×10-6m)的细小可吸入颗粒物,其与空气形成的分散系属于胶体 |
11.下列反应中的氨与反应4NH3+5O2═4NO+6H2O中的氨作用相同的是( )
| A. | NaOH+NH4Cl═NaCl+NH3↑+H2O | B. | 2NH3+3CuO═3Cu+N2+3H2O | ||
| C. | 2Na+2NH3═2NaNH2+H2↑ | D. | NH3+CO2+H2O═NH4HCO3 |
18.能正确表示下列反应的离子方程式是( )
| A. | 向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | |
| B. | 实验室制氨气:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | AlCl3溶液中滴加足量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
15.利用某些有机物之间的相互转换可以贮存太阳能,如原降冰片二烯(NBD)经过太阳光照转化成为四环烷(Q).
已知:①C7H8(l)(NBD)+9O2(g)═7CO2(g)+4H2O(g);△H1;
②C7H8(l)(Q)+9O2(g)═7CO2(g)+4H2O(l);△H2;
③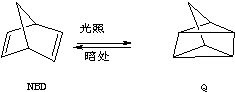 ;△H=+88.62kJ•mol-1
;△H=+88.62kJ•mol-1
下列叙述不正确的是( )
已知:①C7H8(l)(NBD)+9O2(g)═7CO2(g)+4H2O(g);△H1;
②C7H8(l)(Q)+9O2(g)═7CO2(g)+4H2O(l);△H2;
③
 ;△H=+88.62kJ•mol-1
;△H=+88.62kJ•mol-1下列叙述不正确的是( )
| A. | △H1>△H2 | B. | 等质量NBD的能量比Q的能量高 | ||
| C. | NBD比Q稳定 | D. | NBD转化为Q是吸热反应 |
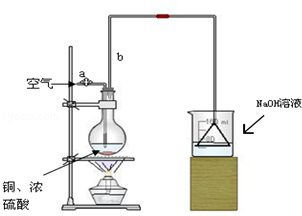 某学校课外活动小组针对教材中铜与浓硫酸反应,提出了“能够与铜反应的硫酸的最低浓度是多少?”的探究课题,并设计了如下方案进行实验:实验试剂:18mol/L硫酸20mL,纯铜粉足量,足量2mol/LNaOH溶液.
某学校课外活动小组针对教材中铜与浓硫酸反应,提出了“能够与铜反应的硫酸的最低浓度是多少?”的探究课题,并设计了如下方案进行实验:实验试剂:18mol/L硫酸20mL,纯铜粉足量,足量2mol/LNaOH溶液.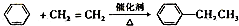
 .
. .
.