13.若NA代表阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 1 mol HClO溶于水电离出NA个H+ | |
| B. | 标准状况下,11.2L的CCl4中含有0.5 NA个分子 | |
| C. | 足量Fe与1 mol Cl2充分反应,转移电子数为2NA | |
| D. | 18.0 g重水(D2O)中所含的电子数为10 NA |
12.下列各反应的产物与反应物用量无关的是( )
| A. | Na2CO3和稀盐酸 | B. | Al2O3和NaOH溶液 | ||
| C. | NH4HCO3和NaOH溶液 | D. | CO2和NaOH溶液 |
11.两种微粒含有相同的质子数和电子数,这两种微粒可能是( )
| A. | 互为同位素的两种原子 | B. | 两种不同元素的原子 | ||
| C. | 一种原子和一种离子 | D. | 一种阴离子和一种阳离子 |
9.新制氯水分别与下列四种物质发生反应,其中能证明新制氯水具有酸性的是( )
| A. | FeCl2 | B. | AgNO3 | C. | KI | D. | Na2CO3 |
8.氨在国民经济中占有重要地位.
(1)合成氨工业中,合成塔中每产生2mol NH3,放出92.2kJ热量.
①工业合成氨的热化学方程式是N2(g)+3H2(g)=2NH3(g)△H=-92.2kJ/mol.
②若起始时向容器内放入1mol N2和3mol H2,达平衡后N2的转化率为20%,则反应放出的热量为Q1kJ,则Q1的数值为18.44;若在同体积的容器中充入2mol N2和6mol H2,达平衡后放出的热量为Q2kJ,则Q2>2Q1(填“>”、“<”或“=”)
③已知:

1mol N-H键断裂吸收的能量约等于391kJ.
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行合成氨反应:N2(g)+3H2(g)?2NH3(g)其化学平衡常数K与温度t的关系如表:请完成下列问题.
①试比较K1.K2的大小,K1>K2(填写“>”.“=”或“<”).
②下列各项能作为判断该反应达到化学平衡状态的依据是c(填序号字母):
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,当测得N2、H2和NH3的物质的量分别为2mol、1mol、2mol时,则此时该反应的v(N2)正> v(N2)逆(填写“>”.“=”或“<”)
(1)合成氨工业中,合成塔中每产生2mol NH3,放出92.2kJ热量.
①工业合成氨的热化学方程式是N2(g)+3H2(g)=2NH3(g)△H=-92.2kJ/mol.
②若起始时向容器内放入1mol N2和3mol H2,达平衡后N2的转化率为20%,则反应放出的热量为Q1kJ,则Q1的数值为18.44;若在同体积的容器中充入2mol N2和6mol H2,达平衡后放出的热量为Q2kJ,则Q2>2Q1(填“>”、“<”或“=”)
③已知:

1mol N-H键断裂吸收的能量约等于391kJ.
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行合成氨反应:N2(g)+3H2(g)?2NH3(g)其化学平衡常数K与温度t的关系如表:请完成下列问题.
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
②下列各项能作为判断该反应达到化学平衡状态的依据是c(填序号字母):
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,当测得N2、H2和NH3的物质的量分别为2mol、1mol、2mol时,则此时该反应的v(N2)正> v(N2)逆(填写“>”.“=”或“<”)
7.室温下,某溶液中由水电离出来的H+和OH-物质的量浓度的乘积为10-24(mol/L)2,下列说法正确的是( )
| A. | HCO3-一定不能大量存在于该溶液中 | |
| B. | NH4+一定不能大量存在于该溶液中 | |
| C. | 该溶液的pH一定为12 | |
| D. | 该溶液中c(H+)=c(OH-) |
5.下列关于铜电极的叙述中不正确的是( )
| A. | 用电解法精炼粗铜时,粗铜作阳极 | |
| B. | 在原电池中,铜电极只能作正极 | |
| C. | 在镀件上镀铜时,金属铜作阳极 | |
| D. | 锌铜原电池(稀硫酸为电解质溶液),铜极上发生还原反应 |
4.I.A-G是几种烃的分子球模型,据此回答下列问题:
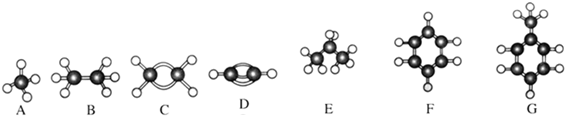
(1)常温下含碳量最高的气态烃是D (填对应字母);
(2)一卤代物种类最多的是G(填对应字母);
(3)写出实验室制取D的化学方程式:CaC2+2H2O→Ca(OH)2+C2H2↑;
(4)写出F发生溴代反应的化学方程式:C6H6+Br2$\stackrel{FeBr_{3}}{→}$C6H5Br+HBr;
Ⅱ、写出除杂的试剂:
Ⅲ、现有分子式为C10H14的一烷基取代苯,已知它有4种同分异构体,请写出其中任意1种的结构简式: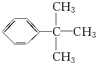 .
.
0 153278 153286 153292 153296 153302 153304 153308 153314 153316 153322 153328 153332 153334 153338 153344 153346 153352 153356 153358 153362 153364 153368 153370 153372 153373 153374 153376 153377 153378 153380 153382 153386 153388 153392 153394 153398 153404 153406 153412 153416 153418 153422 153428 153434 153436 153442 153446 153448 153454 153458 153464 153472 203614

(1)常温下含碳量最高的气态烃是D (填对应字母);
(2)一卤代物种类最多的是G(填对应字母);
(3)写出实验室制取D的化学方程式:CaC2+2H2O→Ca(OH)2+C2H2↑;
(4)写出F发生溴代反应的化学方程式:C6H6+Br2$\stackrel{FeBr_{3}}{→}$C6H5Br+HBr;
Ⅱ、写出除杂的试剂:
| 试剂 | |
| 乙烷混有少量乙烯 | |
| 溴苯混有少量溴单质 |
 .
. 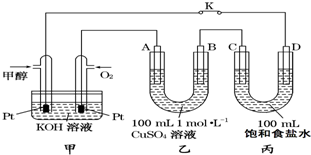 如图是甲醇(CH3OH)燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.
如图是甲醇(CH3OH)燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.