题目内容
10.如表各选项中,不能利用置换反应通过Y得到W的一组化合物是( )| 选项 化合物 | A | B | C | D |
| Y | CuSO4 | Fe2O3 | SiO2 | FeCl3 |
| W | FeSO4 | Al2O3 | CO | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
分析 置换反应为一种单质与一种化合物反应生成另一种单质与另一种化合物的反应,结合物质之间的反应解答.
解答 解:A.铁与硫酸铜反应生成硫酸亚铁和铜,属于置换反应,故A不选;
B.铝与氧化铁反应生成铁和氧化铝,属于置换反应,故B不选;
C.二氧化硅与碳反应生成一氧化碳和硅,属于置换反应,故C不选;
D.氯化铁与铜反应生成氯化亚铁,不属于置换反应,故D选;
故选:D.
点评 本题考查了置换反应,明确物质的性质、发生的反应及置换反应的概念是解题关键,题目难度不大.

练习册系列答案
相关题目
16.下列物质的名称与其化学式相符的是( )
| A. | 液氯(Cl2) | B. | 氯水(Cl2) | C. | 漂白液(NaClO) | D. | 漂白粉[Ca(ClO)2] |
1.今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:第一份加入AgNO3溶液有沉淀产生;第二份加足量NaOH溶液加热后,有刺激性气味的气体放出;第三份加足量BaCl2溶液后,得到白色沉淀,经足量盐酸洗涤,沉淀部分溶解.则下结论正确的是( )
| A. | 该混合液中一定含有:K+、NH4+、CO32-、SO42-,可能含Cl- | |
| B. | 该混合液中一定含有:NH4+、CO32-、SO42-,可能含K+、Cl- | |
| C. | 该混合液中一定含有:NH4+、CO32-、SO42-,可能含Mg2+、K+、Cl- | |
| D. | 该混合液中一定含有:NH4+、SO42-,可能含Mg2+、K+、Cl- |
18.天津是我国研发和生产锂离子电池的重要基地.锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li 被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示.电池反应为CoO2+LiC6 $?_{充电}^{放电}$LiCoO2+C6,下列说法正确的是( )
| A. | 充电时,电池的阳极反应为LiC6-e=Li++C6 | |
| B. | 放电时,电池的正极反应为 CoO2+Li++e-=LiCoO2 | |
| C. | 乙酸、乙醇等含活泼氢的有机物可做该锂离子电池的电解质 | |
| D. | 该锂离子电池的比能量(消耗单位质量电极所释放的电量)比铅蓄电池低 |
5.下列关于铜电极的叙述中不正确的是( )
| A. | 用电解法精炼粗铜时,粗铜作阳极 | |
| B. | 在原电池中,铜电极只能作正极 | |
| C. | 在镀件上镀铜时,金属铜作阳极 | |
| D. | 锌铜原电池(稀硫酸为电解质溶液),铜极上发生还原反应 |
15.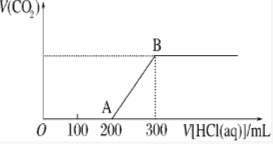 将1.46g NaOH和Na2CO3混合物配成溶液,向溶液中滴加0.1mol•L-1稀盐酸.加入盐酸的体积和生成CO2的物质的量的关系如图所示,则混合物中NaOH和Na2CO3的物质的量之比为( )
将1.46g NaOH和Na2CO3混合物配成溶液,向溶液中滴加0.1mol•L-1稀盐酸.加入盐酸的体积和生成CO2的物质的量的关系如图所示,则混合物中NaOH和Na2CO3的物质的量之比为( )
 将1.46g NaOH和Na2CO3混合物配成溶液,向溶液中滴加0.1mol•L-1稀盐酸.加入盐酸的体积和生成CO2的物质的量的关系如图所示,则混合物中NaOH和Na2CO3的物质的量之比为( )
将1.46g NaOH和Na2CO3混合物配成溶液,向溶液中滴加0.1mol•L-1稀盐酸.加入盐酸的体积和生成CO2的物质的量的关系如图所示,则混合物中NaOH和Na2CO3的物质的量之比为( )| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 2:3 |
2. 向绝热恒容密闭容器中通入SO2和NO2一定条件下使反应SO2(g)+NO2(g)
向绝热恒容密闭容器中通入SO2和NO2一定条件下使反应SO2(g)+NO2(g)
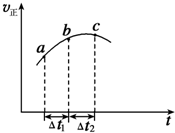
?SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示,
由图可得出的不正确结论是( )
 向绝热恒容密闭容器中通入SO2和NO2一定条件下使反应SO2(g)+NO2(g)
向绝热恒容密闭容器中通入SO2和NO2一定条件下使反应SO2(g)+NO2(g)?SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示,
由图可得出的不正确结论是( )
| A. | 反应在C点达到平衡状态 | |
| B. | 反应物的总能量大于生成物的总能量 | |
| C. | 反应物浓度:a点大于b点 | |
| D. | △t1=△t2时,SO2的转化率:a~b段小于b~c段 |
19.下列实验操作或装置正确的是( )
| A. | 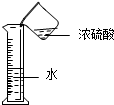 稀释浓硫酸 | B. |  排水集气法收集NO | ||
| C. |  分离水与 酒精 | D. | 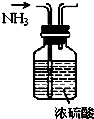 干燥氨气 |
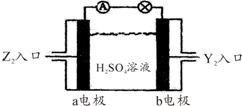 已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子.X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子.请回答下列问题:
已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子.X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子.请回答下列问题: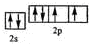 ;
;