20.元素及其化合物的性质是化学研究的主要内容之一.下列叙述正确的是( )
| A. | Na与氧气反应只生成Na2O2 | |
| B. | 将SO2通入过量CaCl2溶液可生成CaSO3沉淀 | |
| C. | 向Fe(NO3)2溶液滴加稀盐酸,溶液变黄色 | |
| D. | 向酚酞试液加足量Na2O2粉末,充分振荡后溶液呈红色 |
19.将Cu片放入0.1mol/LFeCl3溶液中,反应一定时间后取出Cu片,所得溶液Q中的c(Fe3+):c(Fe2+)=2:3,下列有关说法中正确的是( )
| A. | 反应中转移电子为0.04 mol | B. | Q中n(Cu2+):n(Fe2+)=1:2 | ||
| C. | 溶液Q比原溶液增重了 1.28 g | D. | 3c(Fe3+)+2c(Fe2+)+2c(Cu2+)=0.1 mol/L |
18.胶体区别于其它分散系的本质特征是( )
| A. | 胶体稳定 | B. | 胶体有丁达尔效应 | ||
| C. | 胶体能净水 | D. | 胶粒直径在1-100nm之间 |
17.下列化学用语正确的是( )
| A. | 硅的原子结构示意图: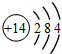 | B. | 乙烯分子比例模型: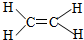 | ||
| C. | 次氯酸分子的电子式: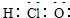 | D. | 乙酸分子的结构简式:C2H4O2 |
15.断开1mol AB(g)分子中的化学键,使其分解生成气态A原子和气态B原子时所吸收的能量称为A-B键的键能.已在H-H键的键能为436kJ•mol-1,H-N键的键能为391kJ•mol-1,根据热化学方程式N2(g)+3H2(g)═2NH3(g)△H=-92kJ•mol-1,推求N≡N键的键能是( )
| A. | 431 kJ•mol-1 | B. | 946 kJ•mol-1 | C. | 649 kJ•mol-1 | D. | 1130 kJ•mol-1 |
14.设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 1.0 L 1.0 mo1•L-1的NaAlO2 水溶液中含有的氧原子数为2 NA | |
| B. | 含有NA个原子的氢气在标准状况下的体积约为22.4 L | |
| C. | 标准状况下,2.24 LCl2与足量水反应转移的电子数为0.2NA | |
| D. | V L a mol•L-1的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目大于3NA |
13.下列实验不能达到预期目的是( )
| A. | 浓、稀HNO3分别与Cu反应比较浓、稀HNO3的氧化性强弱 | |
| B. | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 说明一种沉淀能转化为另一种溶解度更小的沉淀 | |
| C. | 测定等浓度的HCl、HNO3两溶液的pH 比较Cl、N的非金属性强弱 | |
| D. | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 研究浓度对反应速率的影响 |
12.下列离子方程式表达正确的是( )
0 152979 152987 152993 152997 153003 153005 153009 153015 153017 153023 153029 153033 153035 153039 153045 153047 153053 153057 153059 153063 153065 153069 153071 153073 153074 153075 153077 153078 153079 153081 153083 153087 153089 153093 153095 153099 153105 153107 153113 153117 153119 153123 153129 153135 153137 153143 153147 153149 153155 153159 153165 153173 203614
| A. | NaHSO4溶液中滴加入Ba(OH)2溶液至中性H++Ba2++OH-+SO42-═BaSO4↓+H2O | |
| B. | 酸性KMnO4溶液与双氧水反应:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | 钢铁腐蚀时可能发生的正极反应为:4OH-+4e-═2H2O+O2↑ | |
| D. | 将氯气溶于水制备次氯酸:Cl2+H2O?2H++Cl-+ClO- |