3.常温下相关物质的溶度积常数见下表:
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2•2H2O晶体,加入Cu(OH)2或Cu2(OH)2CO3 调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=2.6×10-9mol/L.过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2•2H2O晶体.
(2)由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在干燥的HCl气流中加热脱水.
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.1000mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.(已知:I2+2S2O32-=S4O62-+2I-).
①可选用淀粉溶液作滴定指示剂,滴定终点的现象是蓝色褪去,溶液中30s内不恢复原色.
②CuCl2溶液与KI反应的离子方程式为2Cu2++4I-=2CuI↓+I2.
③该试样中CuCl2•2H2O的质量百分数为95%.
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(2)由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是在干燥的HCl气流中加热脱水.
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.1000mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.(已知:I2+2S2O32-=S4O62-+2I-).
①可选用淀粉溶液作滴定指示剂,滴定终点的现象是蓝色褪去,溶液中30s内不恢复原色.
②CuCl2溶液与KI反应的离子方程式为2Cu2++4I-=2CuI↓+I2.
③该试样中CuCl2•2H2O的质量百分数为95%.
1.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | agC2H4和C3H6的混合物所含原子总数为$\frac{3a{N}_{A}}{14}$ | |
| B. | 1.00mol/LNaCl溶液100mL,含有6.02×1022个NaCl分子 | |
| C. | 300mL2mol/L蔗糖溶液中所含分子数大于0.6NA | |
| D. | 在常温常压下,2.24LSO2与O2混合气体中所含氧原子数为0.2NA |
20.向含有下列离子的溶液中分别加入烧碱固体(溶液的体积变化可忽略),能引起离子浓度增大的是( )
| A. | OH- | B. | Cl- | C. | Cu2+ |
19.化学与生活、生产密切相关,下列说法正确的是( )
0 152939 152947 152953 152957 152963 152965 152969 152975 152977 152983 152989 152993 152995 152999 153005 153007 153013 153017 153019 153023 153025 153029 153031 153033 153034 153035 153037 153038 153039 153041 153043 153047 153049 153053 153055 153059 153065 153067 153073 153077 153079 153083 153089 153095 153097 153103 153107 153109 153115 153119 153125 153133 203614
| A. | 煤的气化和液化都是物理变化,向煤中加入适量CaSO4,可大大减少产物中SO2的量 | |
| B. | BaSO4在医学上用作钡餐,Ba2+对人体无毒 | |
| C. | PM 2.5、二氧化碳都属于空气质量日报的内容 | |
| D. | Na、K合金熔点低,可用作原子反应堆的导热剂 |




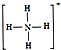 ,白磷(P4)的结构式为
,白磷(P4)的结构式为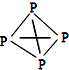 ,请画出N4H44+的结构式
,请画出N4H44+的结构式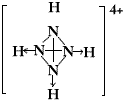 .
.