16.下列实验装置正确且能达到实验目的是( )

| A. | 甲装置:测定盐酸的物质的量浓度 | |
| B. | 乙装置:验证H2SO4、H2CO3、H2SiO3酸性的强弱 | |
| C. | 丙装置:实验室制备乙酸乙酯 | |
| D. | 丁装置:比较碳酸钠和碳酸氢钠的热稳定性 |
15.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,2.24L丙烷中含有的共用电子对数为NA | |
| B. | 25℃时,pH=1的盐酸和醋酸溶液所含H+数均为0.1 NA | |
| C. | 利用双氧水制氧气,每生成1molO2转移电子数为4 NA | |
| D. | 100mL 12mo1•L-1的浓盐酸与足量MnO2加热反应,生成C12分子数为0.3 NA |
13. 利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
(1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
写出氨气经催化氧化完全生成一氧化氮气体和水蒸气的热化学方程式为4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-905.0kJ/mol.
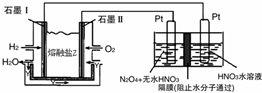
(2)N2O5是一种新型硝化剂,其性质和制备受到人们的关注.现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备N2O5,装置如图所示,其中Y为CO2.写出石墨I电极上发生反应的电极反应式H2+CO32--2e-=CO2+H2O.
在电解池中生成N2O5的电极反应式为N2O4+2HNO3-2e-=2N2O5+2H+.
(3)以甲醇燃料电池为电源,用惰性电极电解饱和NaCl溶液时,每消耗0.2mol CH3OH,阴极产生标况下气体的体积为13.44L.
(4)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g),其化学平衡常数K与温度t的关系如下表:
完成下列问题:
①已知该反应能够自发进行,试比较K1、K2的大小:K1> K2(填“>”、“=”或“<”);
②在同温同压时判断该反应达到化学平衡状态的依据是AC(填序号);
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(5)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似.
①写出盐酸肼第一步水解反应的离子方程式N2H62++H2O?[N2H5•H2O]++H+;
②盐酸肼水溶液中离子浓度的排列顺序不正确的是ABD(填序号).
A.c(Cl-)>c(N2H62+)>c(OH-)>c(H+)
B.c(Cl-)>c([N2H5•H2O+])>c(H+)>c(OH-)
C.2c(N2H62+)+c([N2H5•H2O]+)+c(H+)=c(Cl-)+c(OH-)
D.c(N2H62+)>c(Cl-)>c(H+)>c(OH-)
 利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:(1)已知:N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
写出氨气经催化氧化完全生成一氧化氮气体和水蒸气的热化学方程式为4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-905.0kJ/mol.
(2)N2O5是一种新型硝化剂,其性质和制备受到人们的关注.现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备N2O5,装置如图所示,其中Y为CO2.写出石墨I电极上发生反应的电极反应式H2+CO32--2e-=CO2+H2O.
在电解池中生成N2O5的电极反应式为N2O4+2HNO3-2e-=2N2O5+2H+.
(3)以甲醇燃料电池为电源,用惰性电极电解饱和NaCl溶液时,每消耗0.2mol CH3OH,阴极产生标况下气体的体积为13.44L.
(4)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g),其化学平衡常数K与温度t的关系如下表:
| t/K | 298 | 398 | 498 | … |
| K/(mol•L-1)2 | 4.1×106 | K1 | K2 | … |
①已知该反应能够自发进行,试比较K1、K2的大小:K1> K2(填“>”、“=”或“<”);
②在同温同压时判断该反应达到化学平衡状态的依据是AC(填序号);
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(5)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似.
①写出盐酸肼第一步水解反应的离子方程式N2H62++H2O?[N2H5•H2O]++H+;
②盐酸肼水溶液中离子浓度的排列顺序不正确的是ABD(填序号).
A.c(Cl-)>c(N2H62+)>c(OH-)>c(H+)
B.c(Cl-)>c([N2H5•H2O+])>c(H+)>c(OH-)
C.2c(N2H62+)+c([N2H5•H2O]+)+c(H+)=c(Cl-)+c(OH-)
D.c(N2H62+)>c(Cl-)>c(H+)>c(OH-)
12.已知电离平衡常数:H2CO3>HClO>HCO3-,氧化性:HClO>Cl2>Br2>Fe3+.下列有关的离子方程式正确的是( )
| A. | 向能使pH试纸显深蓝色的溶液中通入少量二氧化碳:OH-+CO2═HCO3- | |
| B. | 向NaClO溶液中加入浓氢溴酸:ClO-+2H++2 Br-═Cl-+Br2+H2O | |
| C. | 向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O═2HClO+CO32- | |
| D. | 向FeBr2溶液中滴加少量Cl2溶液:2 Br-+Cl2═Br2+2Cl- |
10.将直径在1nm~100nm之间的食盐晶体超细粒子分散到酒精中所形成的分散系是( )
| A. | 悬浊液 | B. | 溶液 | C. | 胶体 | D. | 乳浊液 |
9.下列各物质的中心原子采用sp3杂化的是( )
| A. | NH3 | B. | O3 | C. | CO2 | D. | BeCl2 |
8.已知,E(N≡N )=945kJ•mol-1,EH-H=436kJ•mol-1,EN-H=391kJ•mol-1.那么1mol N2与3mol H2合成氨时的能量变化为( )
| A. | 吸收208 kJ的热量 | B. | 放出208 kJ的热量 | ||
| C. | 吸收93 kJ的热量 | D. | 放出93 kJ的热量 |
7.2015年12月12日,《联合国气候变化框架公约》近200个缔约方一致同意通过《巴黎协定》.指出各国应提高力度、加强国际合作,实现全球应对气候变化长期目标.下列做法与社会可持续发展理念相违背的是( )
0 152842 152850 152856 152860 152866 152868 152872 152878 152880 152886 152892 152896 152898 152902 152908 152910 152916 152920 152922 152926 152928 152932 152934 152936 152937 152938 152940 152941 152942 152944 152946 152950 152952 152956 152958 152962 152968 152970 152976 152980 152982 152986 152992 152998 153000 153006 153010 153012 153018 153022 153028 153036 203614
| A. | 改进汽车尾气净化技术,减少大气污染物的排放 | |
| B. | 开发利用可再生能源,减少化石燃料的使用 | |
| C. | 研发可降解高分子材料,减少“白色污染冶 | |
| D. | 过度开采矿物资源,促进地方经济发展 |