题目内容
10.将直径在1nm~100nm之间的食盐晶体超细粒子分散到酒精中所形成的分散系是( )| A. | 悬浊液 | B. | 溶液 | C. | 胶体 | D. | 乳浊液 |
分析 当分散剂是水或其他液体时,如果按照分散质粒子的大小来分类,可以把分散系分为:溶液、胶体和浊液.分散质粒子直径小于1nm的分散系叫溶液,在1nm-100nm之间的分散系称为胶体,而分散质粒子直径大于100nm的分散系叫做浊液.
解答 解:食盐分散到酒精中形成直径1nm~100nm之间的超细粒子的分散系为胶体,
故选C.
点评 本题考查胶体的性质,难度不大,注意同一中物质在不同的分散剂中可以形成不同的分散系.

练习册系列答案
相关题目
1.相同条件下,相同浓度的盐酸分别与镁、铝、铁3种金属恰好完全反应,产生相同体积的氢气(相同状况下),则下列说法正确的是( )
| A. | 开始时,产生氢气的速率相同 | |
| B. | 参加反应的金属的物质的量比为1:1:1 | |
| C. | 所得溶液的质量相等 | |
| D. | 参加反应的金属的质量比为12:9:28 |
18.下列有关实验的说法正确的是( )
| A. | 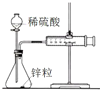 图中测定锌粒与1 mol/L稀硫酸反应速率,只需测定量筒中收集氢气的体积 | |
| B. |  装置中进行50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液测定中和热,使温度计温度升高的热量就是中和反应生成1 mol水的热量 | |
| C. | 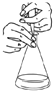 酸碱中和滴定中,可以在滴定过程中用少量水冲洗锥形瓶内壁以减小实验误差 | |
| D. |  滴定管中读数为26.50mL |
5.某有机物的分子模型为  三种不同大小的球代表三种相对大小不同的短周期元素原子,则有关该物质的说法不正确的( )
三种不同大小的球代表三种相对大小不同的短周期元素原子,则有关该物质的说法不正确的( )
 三种不同大小的球代表三种相对大小不同的短周期元素原子,则有关该物质的说法不正确的( )
三种不同大小的球代表三种相对大小不同的短周期元素原子,则有关该物质的说法不正确的( )| A. | 该物质结构简式为:CHCl=CCl2 | B. | 该物质存在顺反异构 | ||
| C. | 该物质可由乙炔通过加成反应得到 | D. | 该物质难溶于水比水重. |
15.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,2.24L丙烷中含有的共用电子对数为NA | |
| B. | 25℃时,pH=1的盐酸和醋酸溶液所含H+数均为0.1 NA | |
| C. | 利用双氧水制氧气,每生成1molO2转移电子数为4 NA | |
| D. | 100mL 12mo1•L-1的浓盐酸与足量MnO2加热反应,生成C12分子数为0.3 NA |
2.下列物质中,属于电解质的是( )
| A. | CO2 | B. | 乙醇 | C. | Na2SO4 | D. | 铜 |
19.氮化铝(AlN)具有耐高温.抗冲击.导热性好等优良性质,被广泛应用于电子工业.陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:
Al2O3+N2+3C$\stackrel{高温}{?}$ 2AlN+3CO下列叙述正确的是( )
Al2O3+N2+3C$\stackrel{高温}{?}$ 2AlN+3CO下列叙述正确的是( )
| A. | 在氮化铝的合成反应中,N2是还原剂,Al2O3氧化剂 | |
| B. | 氮化铝是铝合金中的一种 | |
| C. | 上述反应中每生成2molAlN,N失去6mol电子 | |
| D. | 氮化铝中氮元素的化合价为-3 |
20.下列有关物质的用途错误的是( )
| A. | 水玻璃用作木材防火剂 | |
| B. | 高纯度的硅是制造光导纤维的材料 | |
| C. | 可用氢氟酸刻蚀玻璃 | |
| D. | 氢氧化铝、小苏打可用于治疗胃酸过多症 |
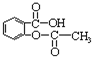 b.烯烃
b.烯烃  c.炔烃
c.炔烃