题目内容
15.NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 标准状况下,2.24L丙烷中含有的共用电子对数为NA | |
| B. | 25℃时,pH=1的盐酸和醋酸溶液所含H+数均为0.1 NA | |
| C. | 利用双氧水制氧气,每生成1molO2转移电子数为4 NA | |
| D. | 100mL 12mo1•L-1的浓盐酸与足量MnO2加热反应,生成C12分子数为0.3 NA |
分析 A、求出丙烷的物质的量,然后根据1mol丙烷中含10mol共用电子对来分析;
B、溶液体积不明确;
C、用双氧水制取氧气,氧元素的价态由-1价变为0价;
D、二氧化锰只能与浓盐酸反应,与稀盐酸不反应.
解答 解:A、标况下2.24L丙烷的物质的量为0.1mol,而1mol丙烷中含10mol共用电子对,故0.1mol丙烷中含1mol共用电子对即NA个,故A正确;
B、溶液体积不明确,故溶液中的氢离子的个数无法计算,故B错误;
C、用双氧水制取氧气,氧元素的价态由-1价变为0价,故当生成1mol氧气时转移2mol电子即2NA个,故C错误;
D、二氧化锰只能与浓盐酸反应,与稀盐酸不反应,故浓盐酸不能反应完全,则生成的氯气分子数小于0.3NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列物质性质与应用对应关系正确的是( )
| A. | 金属钠与TiCl4溶液反应,可以置换出金属钛 | |
| B. | 氢氧化铝具有弱碱性,可用于做胃酸中和剂 | |
| C. | 漂白粉在空气中不稳定,可用于漂白纸张 | |
| D. | 氧化铁能与酸反应,可用于制作红色涂料 |
6.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,22.4 L的H2O中含有的分子数为NA | |
| B. | 7.8g Na2S固体和7.8 g Na2O2固体中含有的阴离子数目均为0.1NA | |
| C. | 46克 Na与足量氧气反应转移的电子数为2NA | |
| D. | 1 L 1mol•L-1 Na2CO3溶液中含有的钠离子数为NA |
10.将直径在1nm~100nm之间的食盐晶体超细粒子分散到酒精中所形成的分散系是( )
| A. | 悬浊液 | B. | 溶液 | C. | 胶体 | D. | 乳浊液 |
20.下列关于安全事故的处理方法中,正确的是 ( )
| A. | 金属钠着火时,立即用水喷洒 | |
| B. | 大量氯气泄漏时,迅速离开现场,并尽量往高处去 | |
| C. | 不慎洒出的酒精在桌上着火时,立即用大量水扑灭 | |
| D. | 少量浓硫酸沾在皮肤上,立即用大量氢氧化钠溶液冲洗 |
4.下列实验能达到预期实验目的是( )
| 实验 | 实验目的 |
| A.测定等物质的量浓度的 CH3COONa和Na2S溶液pH | 比较 CH3COOH和H2S的酸性强弱 |
B.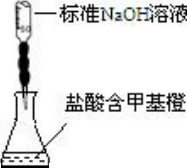 | 测定盐酸的浓度 |
C.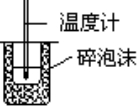 | 测定中和热 |
| D.先用酚酞,后用甲基橙作指示剂,用标准盐酸滴定0.1 mol/L的Na2CO3溶液 | 证明 CO32-水解分两步 |
| A. | A | B. | B | C. | C | D. | D |
5.相同物质的量的下列各烃,完全燃烧消耗氧气最多的是( )
| A. | C2H4 | B. | C2H2 | C. | C3H4 | D. | C2H6 |
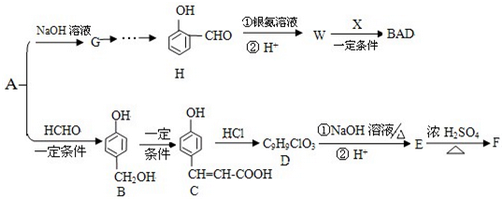
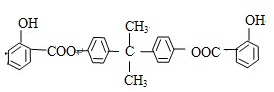
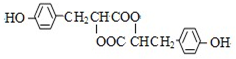
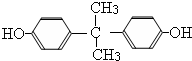 .
.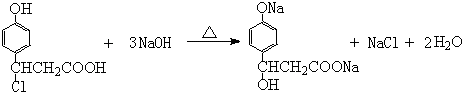 .
.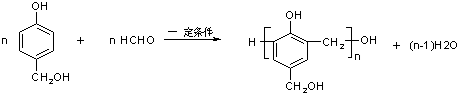 .
. .
.