19.将某元素形成的单质0.1mol与氯气充分反应,生成物的质量比原单质的质量增加了7.1g,这种元素可能是( )
| A. | Na | B. | Fe | C. | Cu | D. | Al |
18.为了验证NaHCO3固体中是否含有Na2CO3,下列实验事实及判断中,正确的是( )
| A. | 溶于水后加石灰水,看有无沉淀 | |
| B. | 加稀盐酸观察是否有气体产生 | |
| C. | 溶于水后加CaCl2溶液,看有无沉淀 | |
| D. | 在无色火焰上灼烧,观察火焰是否呈黄色 |
17.将一小块钠放入下列溶液时,不会出现沉淀的是( )
| A. | 氯化镁溶液 | B. | 饱和氢氧化钠溶液 | ||
| C. | 硫酸铜溶液 | D. | 稀硫酸 |
16.下列物质中既能跟稀H2SO4反应,又能跟氢氧化钠溶液反应的是( )
①Al2O3 ②Al(OH)3 ③(NH4)2CO3 ④NaHCO3 ⑤BaCl2.
①Al2O3 ②Al(OH)3 ③(NH4)2CO3 ④NaHCO3 ⑤BaCl2.
| A. | ①②③④ | B. | ②③④⑤ | C. | ③④⑤ | D. | 全部 |
15.将一定浓度的盐酸倒入盛有块状大理石的烧杯中,若进行如下改变,其中不能使最初的反应速率加快的是( )
| A. | 盐酸的浓度不变,其用量增加一倍 | |
| B. | 盐酸的浓度增加一倍,其用量减少一半 | |
| C. | 使反应在较高的温度下进行 | |
| D. | 盐酸的浓度不变,使块状大理石变成粉末状 |
14.反应4A(s)+3B(g)═2C(g)+D(g),经过2min,B的浓度减少0.6mol/L,对此反应速率的表示正确的是( )
| A. | 在这2 min内A浓度减少了0.8 mol/L | |
| B. | 分别用B、C、D表示的反应速率的比值为3:2:1 | |
| C. | 在2 min末的反应速率,用B表示是:0.3 mol/(L•min) | |
| D. | 在这2 min内用D表示的化学反应速率为:0.2mol/(L•min) |
12.不能用排水收集法收集的气体是( )
| A. | 氢气 | B. | 氧气 | C. | 二氧化氮 | D. | 一氧化氮 |
11.面对日益严重的环境问题,“变废为宝”是化学发展的一个重要方向.例如用废旧酸性锌锰干电池经破碎后的锰粉[含MnO2、MnO(OH)、Zn(NH3)2Cl2、Fe、NH4Cl和炭黑等]制取MnO2及高性能磁性材料碳酸锰(MnCO3),工艺流程如下图所示:
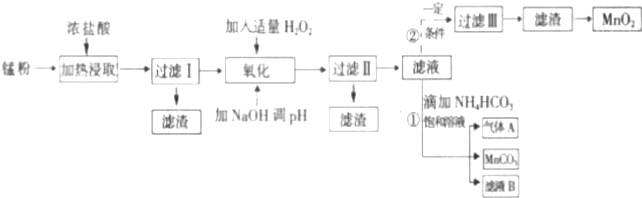
根据以上信息回答问题:
(1)过滤Ⅰ得到的滤渣主要成分是碳黑.
(2)流程中氧化后加入NaOH溶液调节pH的范围为8.5<pH<8.8,其作用是除去Fe3+、Zn2+.
(3)过滤Ⅱ后滤液中阳离子主要是Mn2+.
(4)过滤①中,滤液B含NH4Cl,则生成的气体A是CO2.
(5)请写出酸性锌锰干电池生成锰粉中给出产物的总反应式Zn+2MnO2+2NH4Cl=2MnOOH+Zn(NH3)2Cl2.
(6)将4.00g锰粉完全按照上述工艺流程②生产MnO2,并以此测定其中锰元素的含量.
首先向制取的MnO2中加入过量酸化的0.50mol/LH2C2O4 50.00ml,MnO2完全溶解,并产生A气体,写出该反应的离子方程式:MnO2+H2C2O4+2H+=Mn2++2CO2↑+2H2O.然后用0.1mol/LKMnO4溶液滴定过量的H2C2O4溶液(产物与上反应一致),滴定终点时消耗KMnO4溶液 30.00mL,求锰粉中的锰元素质量分数是24.06%(保留2位有效数字).
0 152806 152814 152820 152824 152830 152832 152836 152842 152844 152850 152856 152860 152862 152866 152872 152874 152880 152884 152886 152890 152892 152896 152898 152900 152901 152902 152904 152905 152906 152908 152910 152914 152916 152920 152922 152926 152932 152934 152940 152944 152946 152950 152956 152962 152964 152970 152974 152976 152982 152986 152992 153000 203614

| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | Zn(OH)2 |
| 沉淀开始时pH | 7.5 | 2.2 | 8.8 | 6.5 |
| 沉淀完全时pH | 9.5 | 3.7 | 10.8 | 8.5 |
(1)过滤Ⅰ得到的滤渣主要成分是碳黑.
(2)流程中氧化后加入NaOH溶液调节pH的范围为8.5<pH<8.8,其作用是除去Fe3+、Zn2+.
(3)过滤Ⅱ后滤液中阳离子主要是Mn2+.
(4)过滤①中,滤液B含NH4Cl,则生成的气体A是CO2.
(5)请写出酸性锌锰干电池生成锰粉中给出产物的总反应式Zn+2MnO2+2NH4Cl=2MnOOH+Zn(NH3)2Cl2.
(6)将4.00g锰粉完全按照上述工艺流程②生产MnO2,并以此测定其中锰元素的含量.
首先向制取的MnO2中加入过量酸化的0.50mol/LH2C2O4 50.00ml,MnO2完全溶解,并产生A气体,写出该反应的离子方程式:MnO2+H2C2O4+2H+=Mn2++2CO2↑+2H2O.然后用0.1mol/LKMnO4溶液滴定过量的H2C2O4溶液(产物与上反应一致),滴定终点时消耗KMnO4溶液 30.00mL,求锰粉中的锰元素质量分数是24.06%(保留2位有效数字).
 的合成路线如下:
的合成路线如下:
 中含有的官能团名称为硝基,氟原子.
中含有的官能团名称为硝基,氟原子. 一定条件下形成聚合物的结构简式为
一定条件下形成聚合物的结构简式为 .
.