20.设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 12.0g熔融的NaHSO4中含有的阳离子数为0.2NA | |
| B. | Na2O2与足量CO2反应生成2.24LO2,转移电子数为0.2NA | |
| C. | 4.6gNO2和N2O4混合物中含有的原子总数为0.3NA | |
| D. | 用惰性电极电解1L浓度均为2mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2NA个电子转移时,理论上阴极析出6.4g金属 |
19.下列说法正确的是( )
| A. | 青铜是我国使用最早的合金,也是目前使用最广泛的合金 | |
| B. | 不管哪种铜合金都含有铜元素,所以它们的性质也和金属铜一样 | |
| C. | 铝合金的硬度比金属铝大 | |
| D. | 生铁的熔点高于纯铁 |
18.某有机分子中含有一个C6H5-,一个-C6H4-,一个-CH2-,一个-OH,则该有机物属于酚类的结构可能有( )
| A. | 3种 | B. | 6种 | C. | 9种 | D. | 12种 |
17.下列化学反应中,既是置换反应又是氧化还原反应的是( )
| A. | 2Al+6HCl═2 AlCl3+3H2 | B. | 4Na+O2═2Na2O | ||
| C. | MgO+H2SO4═MgSO4+2H2O | D. | Ba(OH)2+H2SO4═BaSO4↓+2H2O |
16.下列物质属于电解质的是( )
| A. | NaCl溶液 | B. | 酒精 | C. | HCl | D. | H2 |
15.元素周期表的形式多种多样,如图是扇形元素周期表的一部分,对比中学常见元素周期表,分析其元素的填充规律,判断下列说法正确的是( )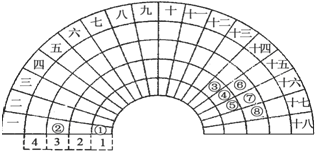

| A. | ③元素形成的单质晶体均属于原子晶体 | |
| B. | ④元素的气态氢化物易液化,是因为其分子间存在氢键 | |
| C. | ②、⑦、⑧对应的简单离子半径依次减小 | |
| D. | ②⑤⑦三种元素形成的盐溶液在25℃时的pH值为7 |
12.能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是( )
| A. | 向水中投入一小块金属钠 | B. | 将水加热煮沸 | ||
| C. | 向水中通入HCl气体 | D. | 向水中加食盐晶体 |
11.已知在1.01×105 Pa、298K条件下,2mol氢气燃烧生成液态水放出484kJ热量,下列表示氢气燃烧热的热化学方程式的是( )
0 152670 152678 152684 152688 152694 152696 152700 152706 152708 152714 152720 152724 152726 152730 152736 152738 152744 152748 152750 152754 152756 152760 152762 152764 152765 152766 152768 152769 152770 152772 152774 152778 152780 152784 152786 152790 152796 152798 152804 152808 152810 152814 152820 152826 152828 152834 152838 152840 152846 152850 152856 152864 203614
| A. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=+242 kJ•mol-1 | B. | 2H2(g)+O2(g)═2H2O(l)△H=-484 kJ•mol-1 | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242 kJ•mol-1 | D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-242 kJ•mol-1 |