6.下列说法正确的是( )
| A. | 葡萄糖可通过酒化酶水解生成酒精 | |
| B. | 分子式为CH4O和C2H6O的物质一定互为同系物 | |
| C. | 向植物油中加入酸性高锰酸钾紫色溶液,振荡后,酸性高锰酸钾溶液颜色褪去 | |
| D. | 淀粉溶液与稀硫酸溶液共热,再加入新制氢氧化铜悬浊液加热,无红色沉淀,则可证明淀粉没有水解 |
5.A、B、C、D、E是元素周期表中前18号元素,原子序数依次增大,他们可组成离子化合物C2B和共价化合物DB3、AE4,已知B、D同主族,C、D、E同周期.下列说法不正确的是( )
| A. | 原子半径C>D>E | |
| B. | A2E6分子中各原子均满足8电子结构 | |
| C. | 气态氢化物的稳定性HmE>HnD | |
| D. | B、C形成的化合物中只可能存在离子键 |
4.化学与人类的生产、生活密切相关,下列说法正确的是( )
| A. | 在空气中,钢铁制品和铝制品都容易发生吸氧腐蚀 | |
| B. | 聚乙烯塑料易老化,是因为发生了加成反应 | |
| C. | 食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质 | |
| D. | 空气质量指标中有一项指标名称为PM2.5,指的是空气中直径≤2.5微米的固体或液体的总称 |
3.实验室合成环己酮的反应、装置示意图及有关数据如下:
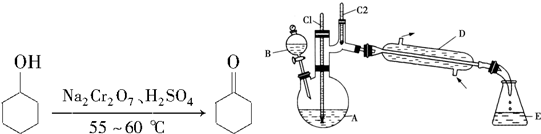
环己醇、环己酮、饱和食盐水和水的部分物理性质见下表
注:括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点.
(1)酸性Na2Cr2O7溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多.实验中通过装置B将酸性Na2Cr2O7溶液(查资料可知Cr是重金属元素,具有致癌性)加到盛有环己醇的A中,在55~60℃进行反应.反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物.
①如何滴加酸性Na2Cr2O7溶液打开分液漏斗上边的玻璃塞,(或含有铬元素的物质)拧开下边的活塞,缓慢滴加,用漂粉精和冰醋酸代替酸性Na2Cr2O7溶液也可氧化环己醇制环己酮,用漂粉精和冰醋酸氧化突出的优点是避免使用有致癌危险的Na2Cr2O7(或避免使用含有致癌性铬元素的物质).
②蒸馏不能分离环己酮和水的原因是环己酮和水形成具有固定组成的恒沸物一起蒸出.
(2)环己酮的提纯需要经过以下一系列的操作:a.蒸馏,收集151~156℃馏分,b.过滤,c.在收集到的馏分中加NaCl固体至饱和,静置,分液,d.加入无水MgSO4固体,除去有机物中少量水.
①上述操作的正确顺序是cdba(填字母).
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有漏斗、分液漏斗.
③在上述操作c中,加入NaCl固体的作用是增加水层的密度,有利于分层,减小产物的损失.

环己醇、环己酮、饱和食盐水和水的部分物理性质见下表
| 物质 | 沸点(℃) | 密度(g•cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8) | 0.962 4 | 能溶于水 |
| 环己酮 | 155.6(95) | 0.947 8 | 微溶于水 |
| 饱和食盐水 | 108.0 | 1.330 1 | |
| 水 | 100.0 | 0.998 2 |
(1)酸性Na2Cr2O7溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多.实验中通过装置B将酸性Na2Cr2O7溶液(查资料可知Cr是重金属元素,具有致癌性)加到盛有环己醇的A中,在55~60℃进行反应.反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物.
①如何滴加酸性Na2Cr2O7溶液打开分液漏斗上边的玻璃塞,(或含有铬元素的物质)拧开下边的活塞,缓慢滴加,用漂粉精和冰醋酸代替酸性Na2Cr2O7溶液也可氧化环己醇制环己酮,用漂粉精和冰醋酸氧化突出的优点是避免使用有致癌危险的Na2Cr2O7(或避免使用含有致癌性铬元素的物质).
②蒸馏不能分离环己酮和水的原因是环己酮和水形成具有固定组成的恒沸物一起蒸出.
(2)环己酮的提纯需要经过以下一系列的操作:a.蒸馏,收集151~156℃馏分,b.过滤,c.在收集到的馏分中加NaCl固体至饱和,静置,分液,d.加入无水MgSO4固体,除去有机物中少量水.
①上述操作的正确顺序是cdba(填字母).
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有漏斗、分液漏斗.
③在上述操作c中,加入NaCl固体的作用是增加水层的密度,有利于分层,减小产物的损失.
20.某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、Na2SO4、FeO、Fe2O3中的若干种,某同学为确定该固体粉末的成分,取甲进行连续实验,实验过程及现象如下:
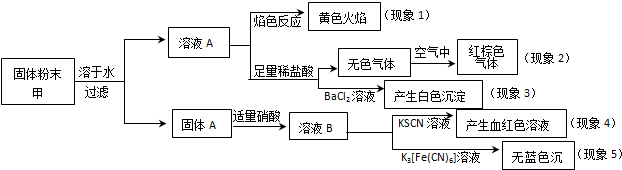
该同学得出的结论正确的是( )

该同学得出的结论正确的是( )
| A. | 根据现象1可推出该固体粉末中含有钠元素,但一定不含钾元素 | |
| B. | 根据现象2可推出该固体粉末中一定不含有NaNO2 | |
| C. | 根据现象3可推出该固体粉末中一定含有Na2SO4 | |
| D. | 根据现象4和现象5可推出该固体粉末中一定不含FeO |
19.室温下,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.2mol/LNH3.H2O溶液与0.1mol/L盐酸等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合后呈酸性:c(CH3COOH)>c(CH3COO-) | |
| C. | 等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c (Na+)=c (SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | 0.1mol/L Na2CO3溶液与0.1mol/LNaHSO4溶液等体积混合所得溶液:c(CO32-)+2 c(OH-)═c(HCO3-)+c(H2CO3)+2c(H+) |
18.以乙烷燃料电池为电源进行电解的实验装置如图所示.下列说法正确的是( )
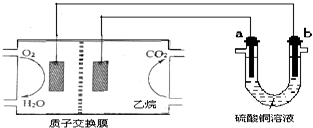

| A. | 燃料电池工作时,正极反应为O2+2H2O+4e-═4OH- | |
| B. | a极是铜,b极是铁时,硫酸铜溶液浓度减小 | |
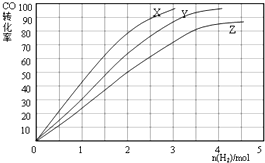
| C. | a、b两极若是石墨,在同温同压下a极产生的气体与电池中消耗的乙烷体积的7/2 | |
| D. | a极是纯铜,b极是粗铜时,a极上有铜析出,b极逐渐溶解,两极质量变化相同 |
17.下列说法不正确的是( )
0 152609 152617 152623 152627 152633 152635 152639 152645 152647 152653 152659 152663 152665 152669 152675 152677 152683 152687 152689 152693 152695 152699 152701 152703 152704 152705 152707 152708 152709 152711 152713 152717 152719 152723 152725 152729 152735 152737 152743 152747 152749 152753 152759 152765 152767 152773 152777 152779 152785 152789 152795 152803 203614
| A. |  的名称为2,3-二甲基戊烷 的名称为2,3-二甲基戊烷 | |
| B. | 18.0g的葡萄糖与乳酸[CH3CH(OH)COOH]混合物完全燃烧消耗氧气13.44L | |
| C. | 结构片段为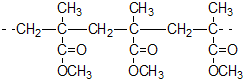 的高聚物,是通过加聚反应生成的 的高聚物,是通过加聚反应生成的 | |
| D. | 化合物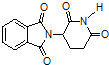 在氢氧化钠溶液中加热后有NH3生成 在氢氧化钠溶液中加热后有NH3生成 |
 .
.