题目内容
4.化学与人类的生产、生活密切相关,下列说法正确的是( )| A. | 在空气中,钢铁制品和铝制品都容易发生吸氧腐蚀 | |
| B. | 聚乙烯塑料易老化,是因为发生了加成反应 | |
| C. | 食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质 | |
| D. | 空气质量指标中有一项指标名称为PM2.5,指的是空气中直径≤2.5微米的固体或液体的总称 |
分析 A、铝的表面有一层致密的氧化膜;
B、聚乙烯中无碳碳双键;
C、生石灰能吸水;
D、PM2.5是指空气中直径小于或等于2.5微米的颗粒物.
解答 解:A、空气中铁制品容易发生吸氧腐蚀,Al因为在空气中表面生成一层致密的氧化膜,故不容易发生吸氧腐蚀,故A错误;
B、要发生加成反应,必须有不饱和键,而聚乙烯中无不饱和键,故不能发生加成反应,故B错误;
C、生石灰有吸水性,主要用于吸水,故应该用作干燥剂,故C错误;
D、PM2.5是指空气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物,富含大量有毒、有害物质,是衡量空气质量的指标之一,故D正确.
故选D.
点评 本题考查了化学知识在生活中的应用,难度不大,应注意的是铝的抗腐蚀能力很强,一般不能发生吸氧腐蚀.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.某溶液能溶解Al(OH)3,则此溶液中可能大量共存的离子组是( )
| A. | Fe3+、NH4+、SCN-、Cl- | B. | K+、Na+、SO42-、HCO3- | ||
| C. | Na+、Ba2+、Cl-、NO3- | D. | A13+、Na+、A1O2-、SO42- |
12.氢气是清洁的能源,也是重要的化工原料,有关氢气的制取研究是一个有趣的课题.根据提供两种制氢方法,完成下列各题:
(1)方法一:H2S热分解法,反应式为:2H2S(g)?2H2(g)+S2(g)△H
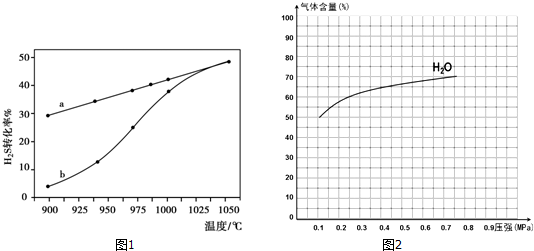
在恒容密闭容器中,控制不同温度进行H2S的分解实验.H2S的起始浓度均为c mol•L-1.不同温度下反应相同时间t后,测得如图1所示H2S转化率曲线图.其中a为平衡转化率与温度关系曲线,b为未达到平衡时转化率与温度的关系曲线.
①△H>0(“>”、“<”或“=”),
②若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则t min内反应速率v(H2)=$\frac{0.4c}{t}$mol•L-1•min-1(用含c、t的代数式表示).
③请说明随温度的升高,曲线b向曲线a逼近的原因:温度升高,反应速率加快,达到平衡所需时间缩短.
(2)方法二:以CaO为吸收体,将生物材质(以C计)与水蒸气反应制取H2.反应装置由气化炉和燃烧炉两个反应器组成,相关反应如下表所示:
①反应C(s)+2H2O(g)+CaO(s)═CaCO3(s)+2H2(g)K=K1•K2•K3.(用K1、K2、K3表示)
②图2为反应I在一定温度下,平衡时各气体体积百分含量随压强变化的关系图2.若反应达某一平衡状态时,测得c(H2O)=2c(H2)=2c(CO)=2mol•L-1,试根据H2O的体积百分含量变化曲线,补充完整CO的变化曲线示意图.
③对于可逆反应C(s)+2H2O(g)+CaO(s)?CaCO3(s)+2H2(g),△H=-87.9kJ•mol-1;采取以下措施可以提高H2产量的是AC.(填字母编号)
A.降低体系的温度
B.使各气体组分浓度均加倍
C.适当增加水蒸气的通入量
D.增加CaO的量,提高CO2的吸收率?
(3)方法二与方法一相比其优点有实现了吸收剂CaO的循环,降低能耗(写一个即可).

(1)方法一:H2S热分解法,反应式为:2H2S(g)?2H2(g)+S2(g)△H
在恒容密闭容器中,控制不同温度进行H2S的分解实验.H2S的起始浓度均为c mol•L-1.不同温度下反应相同时间t后,测得如图1所示H2S转化率曲线图.其中a为平衡转化率与温度关系曲线,b为未达到平衡时转化率与温度的关系曲线.
①△H>0(“>”、“<”或“=”),
②若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则t min内反应速率v(H2)=$\frac{0.4c}{t}$mol•L-1•min-1(用含c、t的代数式表示).
③请说明随温度的升高,曲线b向曲线a逼近的原因:温度升高,反应速率加快,达到平衡所需时间缩短.
(2)方法二:以CaO为吸收体,将生物材质(以C计)与水蒸气反应制取H2.反应装置由气化炉和燃烧炉两个反应器组成,相关反应如下表所示:
| 流程1:气化炉中产生H2 | 流程2:燃烧炉中CaO再生 |
| 通入水蒸气,主要化学反应: Ⅰ:C(s)+H2O(g)═CO(g)+H2(g) K1 Ⅱ:CO(g)+H2O(g)═CO2(g)+H2(g)K2 Ⅲ:CaO(s)+CO2(g)═CaCO3(s)K3 | 通入纯氧,主要化学反应: IV:C(s)+O2(g)═CO2(g) △H=-393.8kJ•mol-1 V:CaCO3(s)═CaO(s)+CO2(g) |
②图2为反应I在一定温度下,平衡时各气体体积百分含量随压强变化的关系图2.若反应达某一平衡状态时,测得c(H2O)=2c(H2)=2c(CO)=2mol•L-1,试根据H2O的体积百分含量变化曲线,补充完整CO的变化曲线示意图.
③对于可逆反应C(s)+2H2O(g)+CaO(s)?CaCO3(s)+2H2(g),△H=-87.9kJ•mol-1;采取以下措施可以提高H2产量的是AC.(填字母编号)
A.降低体系的温度
B.使各气体组分浓度均加倍
C.适当增加水蒸气的通入量
D.增加CaO的量,提高CO2的吸收率?
(3)方法二与方法一相比其优点有实现了吸收剂CaO的循环,降低能耗(写一个即可).
19.室温下,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.2mol/LNH3.H2O溶液与0.1mol/L盐酸等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合后呈酸性:c(CH3COOH)>c(CH3COO-) | |
| C. | 等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c (Na+)=c (SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | 0.1mol/L Na2CO3溶液与0.1mol/LNaHSO4溶液等体积混合所得溶液:c(CO32-)+2 c(OH-)═c(HCO3-)+c(H2CO3)+2c(H+) |
9.已知:HNO2有氧化性,遇强氧化剂显还原性.某溶液中可能含有大量CO32-、S2-、SO32-、SO42-、NO3-、NO2-、OH-等阴离子.为检测上述阴离子,某研究性小组设计了下列实验:
①取少量吸收液于试管中,加入过量的稀盐酸,产生淡黄色浑浊和气体,将所得的气体依次通入品红溶液、足量酸性KMnO4溶液和澄清石灰水,品红褪色,石灰水变浑浊
②另取少量待测液于试管中,加入过量的KClO3固体、AgNO3和稀硝酸,有白色沉淀产生
③另取少量待测液于试管中,酸化后再加入淀粉KI溶液,呈蓝色
④另取少量待测液于试管中,加入足量的BaCl2溶液和稀盐酸,有白色沉淀产生
下列说法正确的是( )
①取少量吸收液于试管中,加入过量的稀盐酸,产生淡黄色浑浊和气体,将所得的气体依次通入品红溶液、足量酸性KMnO4溶液和澄清石灰水,品红褪色,石灰水变浑浊
②另取少量待测液于试管中,加入过量的KClO3固体、AgNO3和稀硝酸,有白色沉淀产生
③另取少量待测液于试管中,酸化后再加入淀粉KI溶液,呈蓝色
④另取少量待测液于试管中,加入足量的BaCl2溶液和稀盐酸,有白色沉淀产生
下列说法正确的是( )
| A. | 由①可推测溶液中一定含大量CO32-、S2-、SO32-、NO3- | |
| B. | 由②可推测溶液中一定含大量NO2- | |
| C. | 由③可推测溶液中一定含大量NO3- | |
| D. | 由实验④难以推测溶液中一定含大量SO42- |
1.合成氨原料可以由天然气制取,其主要反应为:CH4(g)+H2O(g)→CO(g)+3H2(g)
(1)1m3(标准状况)CH4按上式完全反应,产生H2134mol.
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应.1m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为3<V<4.
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
该富氧空气中O2和N2的体积比V(O2)/V(N2)=$\frac{2}{3}$.
(4)若CH4和H2O(g)及富氧空气混合反应的产物中,$\frac{V(H_{2})}{V(N_{2})}$=3:1(合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为(3-7a):3.
(1)1m3(标准状况)CH4按上式完全反应,产生H2134mol.
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应.1m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为3<V<4.
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
| 气体 | CO | H2 | N2 | O2 |
| 体积(L) | 25 | 60 | 15 | 2.5 |
(4)若CH4和H2O(g)及富氧空气混合反应的产物中,$\frac{V(H_{2})}{V(N_{2})}$=3:1(合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为(3-7a):3.
2.亚氯酸钠是一种高效氧化型漂白剂,主要用于棉纺、亚麻、纸浆等漂白.亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是毒性很大的气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).在25℃时,下列分析正确的是( )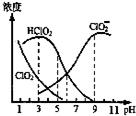

| A. | 使用该漂白剂的最佳pH为3 | |
| B. | pH=5时,溶液中$\frac{c(Cl{{O}_{2}}^{-})}{c(HCl{O}_{2})}$═$\frac{1}{10}$ | |
| C. | pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c( ClO2-)>c( ClO2)>c( Cl-) | |
| D. | NaClO2溶液加水稀释所有离子浓度均减小 |