18.二甲醚(DME)被誉为“21世纪的清洁燃料”.由合成气制备二甲醚的主要原理如下:
反应Ⅰ:CO(g)+2H2(g)?CH3OH(g)△H1
反应Ⅱ:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2
反应Ⅲ:2CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H3
相关反应在不同温度时的平衡常数及其大小关系如下表所示
回答下列问题:
(1)反应Ⅰ的△S<0(填“>”或“<”);反应Ⅱ的平衡常数表达式为$\frac{c(C{H}_{3}OC{H}_{3})×c({H}_{2}O)}{{c}^{2}(C{H}_{3}OH)}$,反应Ⅲ是放热反应(填“吸热”或“放热”).
(2)在合成过程中,因为有CO(g)+H2O(g)?CO2(g)+H2(g)反应发生,所以能提高CH3OCH3的产率,原因是反应消耗了H2O(g)有利于反应Ⅱ、Ⅲ正向移动;同时此反应生成了H2,有利于反应I、Ⅲ正向移动.
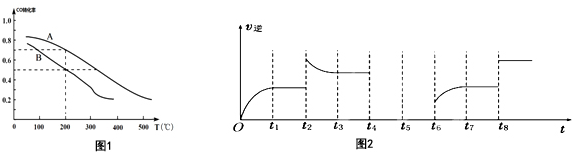
(3)如图1两条曲线分别表示反应I(按物质的量比:n(CO):n(H2)=1:2)中压强为0.1MPa和5.0MPa下CO转化率随温度的变化关系,计算压强为0.1MPa、温度为200℃时,平衡混合气中甲醇的物质的量分数是25%.
(4)反应Ⅲ逆反应速率与时间的关系如图2所示:
①试判断t2时改变的条件是升高温度或增大生成物浓度.
②若t4扩大容器体积,t5达到平衡,t6时增大反应物浓度,请在图2中画出t4-t6的变化曲线.
反应Ⅰ:CO(g)+2H2(g)?CH3OH(g)△H1
反应Ⅱ:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2
反应Ⅲ:2CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H3
相关反应在不同温度时的平衡常数及其大小关系如下表所示
| 温度/K | 反应Ⅰ | 反应Ⅱ | 已知: K1>K2>K1′>K2′ |
| 298 | K1 | K2 | |
| 328 | K1′ | K2′ |
(1)反应Ⅰ的△S<0(填“>”或“<”);反应Ⅱ的平衡常数表达式为$\frac{c(C{H}_{3}OC{H}_{3})×c({H}_{2}O)}{{c}^{2}(C{H}_{3}OH)}$,反应Ⅲ是放热反应(填“吸热”或“放热”).
(2)在合成过程中,因为有CO(g)+H2O(g)?CO2(g)+H2(g)反应发生,所以能提高CH3OCH3的产率,原因是反应消耗了H2O(g)有利于反应Ⅱ、Ⅲ正向移动;同时此反应生成了H2,有利于反应I、Ⅲ正向移动.
(3)如图1两条曲线分别表示反应I(按物质的量比:n(CO):n(H2)=1:2)中压强为0.1MPa和5.0MPa下CO转化率随温度的变化关系,计算压强为0.1MPa、温度为200℃时,平衡混合气中甲醇的物质的量分数是25%.
(4)反应Ⅲ逆反应速率与时间的关系如图2所示:
①试判断t2时改变的条件是升高温度或增大生成物浓度.
②若t4扩大容器体积,t5达到平衡,t6时增大反应物浓度,请在图2中画出t4-t6的变化曲线.

17.以下化学方程式中水只作为氧化剂的是( )
| A. | NaH+H2O═NaOH+H2↑ | B. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | ||
| C. | F2+H2O═2HF+O2↑ | D. | Cl2+H2O?HCl+HClO |
15. 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成化学式为Z2T的离子化合物.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成化学式为Z2T的离子化合物.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成化学式为Z2T的离子化合物.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成化学式为Z2T的离子化合物.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )| A. | 原子半径和离子半径均满足:Y<Z | |
| B. | 最高价氧化物对应的水化物的酸性:T<R | |
| C. | 气态氢化物的稳定性:Y>T | |
| D. | 由X、Y、Z、T四种元素组成的化合物水溶液一定呈中性 |
14.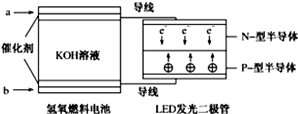 下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )
下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )
 下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )
下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )| A. | 氢氧燃料电池中OH-向b极移动 | |
| B. | 该装置中只涉及两种形式的能量转化 | |
| C. | H2在负极发生氧化反应 | |
| D. | P一型半导体连接电池负极 |
13.一种“即食即热快餐”适合外出旅行时使用.其内层是用铝箔包裹的,并已加工好的真空包装食品.外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两包的化学物质反应,此时便可以对食物进行加热,这两包化学物质最合适的选择是( )
| A. | 硫酸与水 | B. | 氯化钠与水 | C. | 熟石灰与水 | D. | 生石灰与水 |
12.聚异丁烯( )是生产汽油清洁剂的中间产物.下列关于聚异丁烯的说法中错误的是( )
)是生产汽油清洁剂的中间产物.下列关于聚异丁烯的说法中错误的是( )
 )是生产汽油清洁剂的中间产物.下列关于聚异丁烯的说法中错误的是( )
)是生产汽油清洁剂的中间产物.下列关于聚异丁烯的说法中错误的是( )| A. | 聚异丁烯可以通过加聚反应制得 | |
| B. | 聚异丁烯的分子式为(C4H8)n | |
| C. | 聚异丁烯能使溴的四氯化碳溶液褪色 | |
| D. | 聚异丁烯完全燃烧生成CO2 和H2O的物质的量相等 |
11.下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述中,不正确的是( )
| A. | 纤维素$\stackrel{水解}{→}$葡萄糖$\stackrel{氧化}{→}$CO2和H2O(释放能量维持生命活动) | |
| B. | 淀粉$\stackrel{水解}{→}$葡萄糖$\stackrel{氧化}{→}$CO2和H2O(释放能量维持生命活动) | |
| C. | 蛋白质$\stackrel{水解}{→}$氨基酸$\stackrel{合成}{→}$人体所需的蛋白质(人体生长发育) | |
| D. | 油脂$\stackrel{水解}{→}$甘油和高级脂肪酸$\stackrel{氧化}{→}$CO2和H2O(释放能量维持生命活动) |
10.在光照条件下,CH4与Cl2能发生取代反应:若将1 mol CH4与Cl2反应,待反应完成后测得四种有机取代物的物质的量之比为:n(CH3Cl):n(CH2Cl2):n(CHCl3):n(CCl4)=4:3:2:1,则消耗的Cl2为( )
| A. | 1.0 mol | B. | 2.0 mol | C. | 3.0 mol | D. | 4.0 mol |
9.下列措施对增大反应速率明显有效的是( )
0 152563 152571 152577 152581 152587 152589 152593 152599 152601 152607 152613 152617 152619 152623 152629 152631 152637 152641 152643 152647 152649 152653 152655 152657 152658 152659 152661 152662 152663 152665 152667 152671 152673 152677 152679 152683 152689 152691 152697 152701 152703 152707 152713 152719 152721 152727 152731 152733 152739 152743 152749 152757 203614
| A. | Na与水反应时增大水的用量 | |
| B. | Fe与稀硫酸反应制取H2 时,改用浓硫酸 | |
| C. | 在K2SO4与BaCl2两溶液反应时,降低温度 | |
| D. | Al与氧气燃烧生成Al2O3,将Al片改为Al粉, |
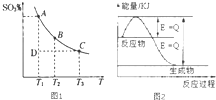 运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.