18.下列叙述中正确的是( )
| A. | 反应N2(g)+3H2(g)═2NH3(g),其他条件不变时充入N2,正反应速率增大,逆反应速率减小 | |
| B. | 常温下,2NO(g)+O2(g)═2NO2(g)能够自发进行,则该反应的△H<0 | |
| C. | 向0.1mol/L CH3COOH溶液中加入少量的冰醋酸,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(O{H}^{-})}$的值变小 | |
| D. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 |
16.绿柱石被国际珠宝界公认为四大名贵宝石之一.主要成分为Be3Al2[Si6O18],因含适量的Cr2O3(0.15~0.6%),而形成祖母绿.试回答下列问题:
(1)基态Al原子中,电子填充的最高能级是3p,基态Cr原子的价电子排布式是3d54s1.
(2)用“>”或“<”填空:
(3)BeCl2分子的空间构型是直线型,它的二聚体Be2Cl4结构如右图所示,其中Be原子的杂化方式是sp3.
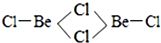
(4)强还原剂LiAlH4能将SiCl4还原成SiH4,试写出SiH4在空气中自燃的化学方程式SiH4+2O2=SiO2+2H2O.
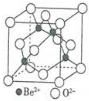
(5)Be的氧化物的立方晶胞结构如右图所示,已知氧化铍晶体的密度为ρg•cm-3,则晶胞连长为$\root{3}{\frac{100}{ρ{N}_{A}}}$cm(设NA为阿伏加德罗常数的值,用含NA、ρ的代数式表示).
(1)基态Al原子中,电子填充的最高能级是3p,基态Cr原子的价电子排布式是3d54s1.
(2)用“>”或“<”填空:
| 第一电离能 | 键能 | 沸点 | 离子半径 |
| Be>B | C-C>Si-Si | H2S<H2O | Al3+<O2- |

(4)强还原剂LiAlH4能将SiCl4还原成SiH4,试写出SiH4在空气中自燃的化学方程式SiH4+2O2=SiO2+2H2O.
(5)Be的氧化物的立方晶胞结构如右图所示,已知氧化铍晶体的密度为ρg•cm-3,则晶胞连长为$\root{3}{\frac{100}{ρ{N}_{A}}}$cm(设NA为阿伏加德罗常数的值,用含NA、ρ的代数式表示).

15.1个SO32-离子恰好将1个XO4-离子还原,则X元素在还原产物中化合价是( )
| A. | +2 | B. | +3 | C. | +4 | D. | +5 |
14.设阿伏加德罗常数的数值为NA,下列叙述正确的是( )
| A. | 0.5 mol•L-1 NaOH溶液中Na+数为0.5NA | |
| B. | 标准状况下,22.4 L四氯化碳含有的分子数为NA | |
| C. | 常温常压下,1mol Na2O2与足量CO2反应,电子转移数为NA | |
| D. | 标准状况下,16 g氧气臭氧的混合气体所含原子数一定为2NA |
13.下列有关化学常识正确的是( )
0 152525 152533 152539 152543 152549 152551 152555 152561 152563 152569 152575 152579 152581 152585 152591 152593 152599 152603 152605 152609 152611 152615 152617 152619 152620 152621 152623 152624 152625 152627 152629 152633 152635 152639 152641 152645 152651 152653 152659 152663 152665 152669 152675 152681 152683 152689 152693 152695 152701 152705 152711 152719 203614
| A. | 钠钾合金可用于中子反应堆作热交换剂 | |
| B. | 氯气本身有毒,因此不能用于药物合成 | |
| C. | 不用氧化镁电解熔融制镁的原因是氧化镁不导电 | |
| D. | 工业高炉炼铁过程中,加石灰石主要是为了制备还原剂 |
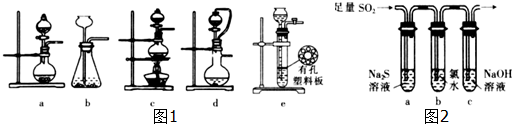
 在化学研究领域,经常需要对一些物质进行性质的确定.如利用下列装置(夹持仪器已略去)测出一定质量镁与盐酸反应放出的气体体积,对金属镁的相对原子质量进行测定,实验步骤如下:
在化学研究领域,经常需要对一些物质进行性质的确定.如利用下列装置(夹持仪器已略去)测出一定质量镁与盐酸反应放出的气体体积,对金属镁的相对原子质量进行测定,实验步骤如下: