题目内容
14.设阿伏加德罗常数的数值为NA,下列叙述正确的是( )| A. | 0.5 mol•L-1 NaOH溶液中Na+数为0.5NA | |
| B. | 标准状况下,22.4 L四氯化碳含有的分子数为NA | |
| C. | 常温常压下,1mol Na2O2与足量CO2反应,电子转移数为NA | |
| D. | 标准状况下,16 g氧气臭氧的混合气体所含原子数一定为2NA |
分析 A、溶液体积不明确;
B、标况下四氯化碳为液态;
C、过氧化钠与二氧化碳的反应为歧化反应;
D、氧气和臭氧均由氧原子构成.
解答 解:A、溶液体积不明确,故溶液中的钠离子的个数无法计算,故A错误;
B、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、过氧化钠与二氧化碳的反应为歧化反应,过氧化钠中氧元素中的价态由-1价变为0价,故1mol过氧化钠反应转移1mol电子即NA个,故C正确;
D、氧气和臭氧均由氧原子构成,故16g混合物中含有的氧原子的物质的量为n=$\frac{16g}{16g/mol}$=1mol,个数为NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
20.合成氨是人类科学技术上的一项重大突破,工业上以天然气为原料合成氨.其生产
工艺如下:造气阶段→转化阶段→分离净化→合成阶段
(1)造气阶段的反应为:CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.1kJ/mol
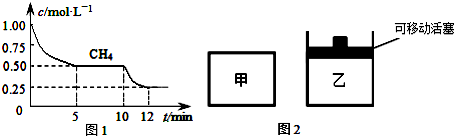
①在一个密闭容器中进行上述反应,测得CH4的物质的量浓度随反应时间的变化如下图1所示,10min时,改变的外界条件可能是升高温度等.
②如图2所示,在初始容积相等的甲、乙两容器中分别充入等物质的量的CH4和H2O.在相同温度下发生反应,并维持反应过程中温度不变.则达到平衡时,两容器中CH4的转化率大小关系为:α甲(CH4)<α乙(CH4)
(2)转化阶段发生的可逆反应为:CO(g)+H2O(g)?CO2(g)+H2(g),在一定温度下,反应的平衡常数为K=1.某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
此时反应中正、逆反应速率的关系式是a(填序号).
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
(3)合成氨反应为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
根据勒夏特列原理,简述提高合成氨原料转化率的一种方法增大压强或降低温度或分离液氨.
(4)工业合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.在某压强恒定的密闭容器中加入2mol N2和4mol H2,达到平衡时,N2的转化率为50%,体积变为10L.求:
①该条件下的平衡常数为400;
②若向该容器中加入a mol N2、b mol H2、c mol NH3,且a、b、c 均大于0,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同.反应放出的热量<(填“>”“<”或“=”)92.4kJ.
③在一定温度下,在一个容积不变的密闭容器中,发生合成氨反应,下列能判断该反应达到化学平衡状态的是cd
a.v(N2)=3v(NH3) b.混合气体的密度不随时间改变
c.混合气体的平均相对分子质量不随时间改变 d.容器中的压强不随时间改变
e.c(N2)=c(NH3)
工艺如下:造气阶段→转化阶段→分离净化→合成阶段
(1)造气阶段的反应为:CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.1kJ/mol
①在一个密闭容器中进行上述反应,测得CH4的物质的量浓度随反应时间的变化如下图1所示,10min时,改变的外界条件可能是升高温度等.
②如图2所示,在初始容积相等的甲、乙两容器中分别充入等物质的量的CH4和H2O.在相同温度下发生反应,并维持反应过程中温度不变.则达到平衡时,两容器中CH4的转化率大小关系为:α甲(CH4)<α乙(CH4)

(2)转化阶段发生的可逆反应为:CO(g)+H2O(g)?CO2(g)+H2(g),在一定温度下,反应的平衡常数为K=1.某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
(3)合成氨反应为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
根据勒夏特列原理,简述提高合成氨原料转化率的一种方法增大压强或降低温度或分离液氨.
(4)工业合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.在某压强恒定的密闭容器中加入2mol N2和4mol H2,达到平衡时,N2的转化率为50%,体积变为10L.求:
①该条件下的平衡常数为400;
②若向该容器中加入a mol N2、b mol H2、c mol NH3,且a、b、c 均大于0,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同.反应放出的热量<(填“>”“<”或“=”)92.4kJ.
③在一定温度下,在一个容积不变的密闭容器中,发生合成氨反应,下列能判断该反应达到化学平衡状态的是cd
a.v(N2)=3v(NH3) b.混合气体的密度不随时间改变
c.混合气体的平均相对分子质量不随时间改变 d.容器中的压强不随时间改变
e.c(N2)=c(NH3)
1.下列实验操作中,不正确的是( )
| A. | 金属钠在用小刀切割后,剩余的钠应放回煤油中 | |
| B. | 焰色反应实验前,铂丝应先用盐酸洗涤后灼烧至无色,焰色反应是一种物理变化 | |
| C. | 实验室制备氢氧化亚铁时,滴加氢氧化钠溶液的胶头滴管伸入液面下 | |
| D. | 将烧碱溶液保存在磨口的细口玻璃瓶中 |
2.如图是侯氏制碱法在实验室进行模拟实验的生产流程示意图:
饱和食盐水$→_{Ⅰ}^{通入足量的气体A}$A和食盐饱和溶液$→_{Ⅱ}^{通入过量的气体B}$悬浊液$→_{Ⅲ}^{过滤}$晶体$\overrightarrow{Ⅳ}$纯碱
则下列叙述错误的是( )
饱和食盐水$→_{Ⅰ}^{通入足量的气体A}$A和食盐饱和溶液$→_{Ⅱ}^{通入过量的气体B}$悬浊液$→_{Ⅲ}^{过滤}$晶体$\overrightarrow{Ⅳ}$纯碱
则下列叙述错误的是( )
| A. | A气体是NH3,B气体是CO2 | |
| B. | 侯氏制碱法的工艺过程应用了物质溶解度的差异 | |
| C. | 第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒 | |
| D. | 第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶 |
6.加热13.7g Na2CO3和NaHCO3的固体混合物至质量不再发生变化,剩余固体质量为10.6g,则混合物中Na2CO3的质量分数约为( )
| A. | 84% | B. | 50% | C. | 16% | D. | 39% |
3.将浓度为0.1mol•L-1HF溶液加水不断稀释,下列各量始终保持增大的是( )
| A. | [H+] | B. | Ka(HF) | C. | $\frac{[{F}^{-}]}{[{H}^{+}]}$ | D. | $\frac{[{H}^{+}]}{[HF]}$ |
4.下列说法正确的是( )
| A. | 分子式为C7H8O,且含苯环的有机化合物有4种 | |
| B. | 乙醇能使酸性高锰酸钾溶液褪色 | |
| C. | 向无水乙醇中加入浓H2SO4,加热至170℃,产生的使酸性KMnO4溶液褪色的气体只是乙烯 | |
| D. | 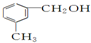 遇FeCl3溶液可显紫色 遇FeCl3溶液可显紫色 |
 在化学研究领域,经常需要对一些物质进行性质的确定.如利用下列装置(夹持仪器已略去)测出一定质量镁与盐酸反应放出的气体体积,对金属镁的相对原子质量进行测定,实验步骤如下:
在化学研究领域,经常需要对一些物质进行性质的确定.如利用下列装置(夹持仪器已略去)测出一定质量镁与盐酸反应放出的气体体积,对金属镁的相对原子质量进行测定,实验步骤如下: