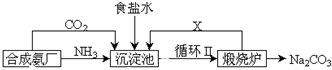
18.钠及其化合物具有广泛的用途.
(1)常温下,浓度均为 0.1mol•L-1 的下列五种钠盐溶液的 pH 如表;
上述盐溶液中的阴离子,结合H+能力最强的是CO32-,根据表中数据,浓度均为0.01mol•L-1 的下列四种酸的溶液分别稀释 100倍,pH变化最大的是C(填编号).
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)有①100ml 0.1mol/L NaHCO3②100ml 0.1mol/L Na2CO3 两种溶液:
溶液中水电离出的H+个数:①<②(填“>”、“=”或“<”,下同).
溶液中阴离子的物质的量浓度之和:①>②.
( 3 ) NaHCO3是一种强(填“强”或“弱”)电解质;写出HCO${\;}_{3}^{-}$水解的离子方程式:HCO3-+H2O?H2CO3+OH-,常温下,0.1mol•L-1NaHCO3溶液的pH大于8,则溶液中 Na+、HCO3-、H2CO3、CO32-、OH-五种微粒的浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-).
(4)实验室中常用 NaOH 来进行洗气和提纯.
①当 150ml 1mol/L 的 NaOH 溶液吸收标准状况下 2.24LCO2时,所得溶液中各离子浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
②几种离子开始沉淀时的 PH 如表:
当向含相同浓度 Cu2+、Mg2+、Fe2+离子的溶液中滴加 NaOH 溶液时,Cu2+(填离子符号)先沉淀,Ksp[Fe(OH)2]<Ksp[Mg(OH)2](填“>”、“=”或“<”),要使 0.2mol/L 硫酸铜溶液中 Cu2+沉淀较为完全(使 Cu2+浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液使溶液pH为6.
(KspCu(OH)2=2×10mol•L )
(1)常温下,浓度均为 0.1mol•L-1 的下列五种钠盐溶液的 pH 如表;
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)有①100ml 0.1mol/L NaHCO3②100ml 0.1mol/L Na2CO3 两种溶液:
溶液中水电离出的H+个数:①<②(填“>”、“=”或“<”,下同).
溶液中阴离子的物质的量浓度之和:①>②.
( 3 ) NaHCO3是一种强(填“强”或“弱”)电解质;写出HCO${\;}_{3}^{-}$水解的离子方程式:HCO3-+H2O?H2CO3+OH-,常温下,0.1mol•L-1NaHCO3溶液的pH大于8,则溶液中 Na+、HCO3-、H2CO3、CO32-、OH-五种微粒的浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-).
(4)实验室中常用 NaOH 来进行洗气和提纯.
①当 150ml 1mol/L 的 NaOH 溶液吸收标准状况下 2.24LCO2时,所得溶液中各离子浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
②几种离子开始沉淀时的 PH 如表:
| 离子 | Fe 2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
(KspCu(OH)2=2×10mol•L )
15.用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )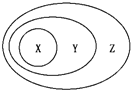

| X | Y | Z | |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 溶液 | 分散系 | 混合物 |
| B | 铜 | 金属元素 | 元素 |
| C | 强电解质 | 电解质 | 化合物 |
| D | 置换反应 | 氧化还原反应 | 离子反应 |
| A. | A | B. | B | C. | C | D. | D |
14.CuSO4、Fe2(SO4)3的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6mol•L-1,则此溶液最多溶解铁粉的质量为( )
| A. | 5.6 g | B. | 11.2 g | C. | 22.4 g | D. | 20.16 g |
13. 以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V (g)(标准状况)的关系如图所示.下列说法中,正确的是( )
以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V (g)(标准状况)的关系如图所示.下列说法中,正确的是( )
 以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V (g)(标准状况)的关系如图所示.下列说法中,正确的是( )
以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体体积V (g)(标准状况)的关系如图所示.下列说法中,正确的是( )| A. | 电解前CuSO4溶液的物质的量浓度为2mol/L | |
| B. | 电解后所得溶液中c(H+)=2mol/L | |
| C. | 当n(e-)=0.6mol时,V(H2):V(O2)=2:3 | |
| D. | 向电解后的溶液中加入16gCuO,则溶液可恢复为电解前的浓度 |
12.25℃时,将25.00mLHgI2饱和溶液分数次加入离子交换柱中,进行如下离子交换反应:Hg2+(aq)+2RH(s)=R2Hg(s)+2H+(aq),用洁净的锥形瓶接流出液,待溶液流出后,再用蒸馏水淋洗树脂至流出液呈中性,将洗涤液一并放在锥形瓶中,加入指示剂,用0.0025mol/LNaOH溶液滴定,当达到滴定终点时,用去氢氧化钠溶液20.00mL.结合上述实验数据,下列有关说法正确的是( )
0 152353 152361 152367 152371 152377 152379 152383 152389 152391 152397 152403 152407 152409 152413 152419 152421 152427 152431 152433 152437 152439 152443 152445 152447 152448 152449 152451 152452 152453 152455 152457 152461 152463 152467 152469 152473 152479 152481 152487 152491 152493 152497 152503 152509 152511 152517 152521 152523 152529 152533 152539 152547 203614
| A. | 其他步骤正确,滴定达到终点时,俯视读数,测得c(H+)偏大 | |
| B. | 实验测得25℃时,HgI2的Ksp=4×10-9 | |
| C. | 一定温度下,向HgI2饱和溶液中加入少量Hg(NO3)2溶液,HgI2的Ksp减小 | |
| D. | 温度不变,在t时,向HgI2饱和溶液中加入少量浓KI溶液,离子浓度变化如图所示 |
 实验室配制500mL 0.1mol•L-1的NaCl溶液,有如下操作步骤:
实验室配制500mL 0.1mol•L-1的NaCl溶液,有如下操作步骤: