题目内容
10.实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.(1)在如图所示仪器中,配制上述溶液肯定不需要的是AC(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是烧杯、玻璃棒、500mL容量瓶.
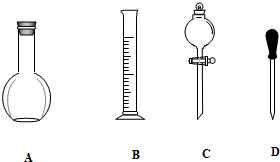
(2)在容量瓶的使用方法中,下列操作不正确的是BCD
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线.
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线.
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀.
(3)根据计算用托盘天平称取的质量为2.0g.在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度小于0.1mol/L(填“大于”“小于”或“等于”).
分析 (1)依据配制一定物质的量浓度溶液的一般步骤选择需要仪器,确定用不到的仪器和缺少的仪器;
(2)依据容量瓶构造及使用方法及注意事项解答;
(3)依据配制溶液体积选择合适的容量瓶,依据m=CVM计算需要溶质的质量;定容时仰视刻度线,导致溶液体积偏大,依据C=$\frac{n}{V}$进行误差判断.
解答 解:(1)配制一定物质的量浓度溶液的一般步骤:计算、称量或者量取、溶解或者稀释、移液、洗涤、定容、摇匀,用到的仪器:托盘天平、药匙、量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,用不到平底烧瓶和分液漏斗,还缺少的仪器:烧杯、玻璃棒、500mL容量瓶;
故答案为:AC;烧杯、玻璃棒、500mL容量瓶;
(2)A.容量瓶带有瓶塞,使用前应检查是否漏水,故A正确;
B.容量瓶用水洗净后,再用待配溶液洗涤,导致溶质的物质的量偏大,溶液浓度偏高,故B错误;
C.容量瓶为精密仪器,不能用来溶解固体,故C错误;
D.容量瓶为精密仪器,不能用来稀释浓溶液,故D错误;
E.定容后,盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀,故E正确;
故选:BCD;
(3)需要0.1mol/LNaOH溶液450mL,应选择500mL容量瓶,实际配制500mL溶液,需要溶质的质量m=0.1mol/L×40g/mol×0.5L=2.0g;定容时仰视刻度线,导致溶液体积偏大,依据C=$\frac{n}{V}$可知溶液浓度偏低,
故答案为:2.0;小于.
点评 本题考查了一定物质的量浓度溶液的配制及误差分析,明确配制原理和操作步骤是解题关键,注意容量瓶构造及使用方法,题目难度不大.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
8.Na2FeO4是一种高效的水处理剂,下列用于解释事实的方程式中,不正确的是( )
| A. | Na2FeO4消毒、杀菌时得到的Fe3+可以净水,Fe3+能产生净水物质的原因是:Fe3++3H2O?Fe(OH)3(胶体)+3H+ | |
| B. | 工业上可用FeCl3、NaOH、NaClO三种物质反应制得Na2FeO4,化学方程式为:2FeCl3+10NaOH+3NaClO═2 Na2FeO4+9NaCl+5H2O | |
| C. | Na2FeO4在酸性溶液中不稳定,与水反应生成Fe3+和O2,离子方程式为:4FeO42-+10H2O═4Fe3++20OH-+3O2↑ | |
| D. | 工业上可用铁做阳极,电解浓NaOH溶液的方法制Na2FeO4,阳极的电极反应为:Fe-6e-+8OH-═FeO42-+4H2O |
9.某些电解质分子的中心原子最外层不足8电子,其电离时结合其他离子使中心原子最外层达到8电子结构.例如硼酸在水中电离方程式为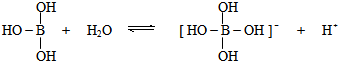 .下列判断正确的是( )
.下列判断正确的是( )
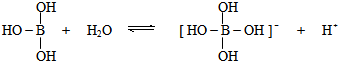 .下列判断正确的是( )
.下列判断正确的是( )| A. | 硼酸是三元酸,抑制水的电离 | |
| B. | 硼酸分子中各原子最外层均达到8电子结构 | |
| C. | 硼酸与NaOH溶液反应的离子方程式:H3BO3+OH-═[B(OH)4]- | |
| D. | 硼酸是两性氢氧化物,也能与强酸溶液反应 |
15.用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )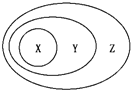

| X | Y | Z | |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 溶液 | 分散系 | 混合物 |
| B | 铜 | 金属元素 | 元素 |
| C | 强电解质 | 电解质 | 化合物 |
| D | 置换反应 | 氧化还原反应 | 离子反应 |
| A. | A | B. | B | C. | C | D. | D |
 ,其与过量的NaOH溶液反应的化学方程式是
,其与过量的NaOH溶液反应的化学方程式是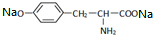 +2H2O.
+2H2O.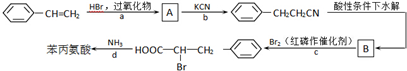
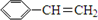 +HBr→
+HBr→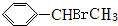 .
. +Br2$\stackrel{红磷}{→}$
+Br2$\stackrel{红磷}{→}$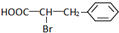 +HBr.
+HBr.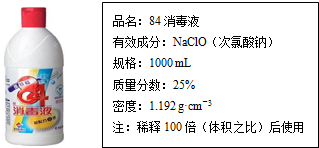
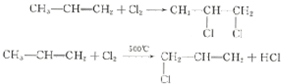
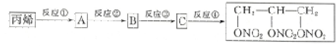
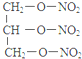 +3H2O.
+3H2O.