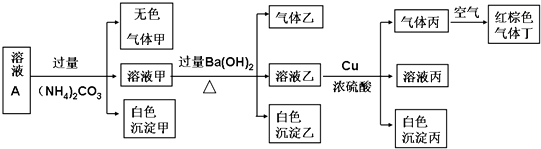
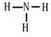10.两种金属的混合物共15g,跟足量的盐酸反应时,恰好得到11.2L氢气(标况).下列各组金属不可能构成上述条件的混合物的是( )
| A. | 镁和银 | B. | 铁和锌 | C. | 铝和铁 | D. | 镁和铁 |
9.已知:2Fe203(s)+3C(s)═3C02(g)+4Fe(s)△H=+468.2kJ.mol-l;
C(s)+02 (g)═C02 (g)△H=-393.5kJ.mol-1;
则4Fe(s)+3O2(g)═2Fe203(s)的△H是( )
C(s)+02 (g)═C02 (g)△H=-393.5kJ.mol-1;
则4Fe(s)+3O2(g)═2Fe203(s)的△H是( )
| A. | -1648.7 kJ.mo1-1 | B. | -1255.3 kJ.mol-1 | ||
| C. | -861.7 kJ.mol-l | D. | +867.1 kJ.mol-1 |
8.甲~庚等元素在元素周期表中的相对位置如下表,己的最高价氧化物对应的水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数,下列判断正确的是( )

| A. | 丙与戊的原子序数相差28 | |
| B. | 气态氢化物的稳定性:庚<己<戊 | |
| C. | 常温下,甲和乙的单质均能与水剧烈反应 | |
| D. | 丁的最高价氧化物可广泛可于太阳能电池 |
7.某实验小组依据反应 AsO${\;}_{4}^{3-}$+2H++2I-?AsO${\;}_{3}^{3-}$+I2+H2O设计如图原电池,探究pH对AsO4氧化性的影响.测得电压与pH的关系如图.下列有关叙述错误的是( )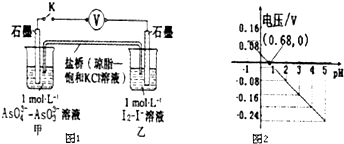

| A. | 调节pH可以改变反应的方向 | |
| B. | pH=0.68 时,反应处于平衡状态 | |
| C. | pH=5 时,负极电极反应式为2I--2e-═I2 | |
| D. | pH>0.68时,氧化性I2>AsO${\;}_{4}^{3-}$ |
5.常温下,pH>7的某溶液中只含有Na+、CH3COO-、H+、OH-四种离子,下列描述正确的是( )
| A. | 该溶液只能由等物质的量浓度、等体积的氢氧化钠溶液和醋酸溶液混合而成 | |
| B. | 该溶液一定由pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合而成 | |
| C. | 该溶液中离子浓度一定为c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 加入一定冰醋酸,c(CH3COO-)可能大于、等于或小于c(Na+) |
3.下列关于反应热的说法正确的是( )
| A. | 当△H为“-”时,表示该反应为吸热反应 | |
| B. | 反应热的大小与反应物所具有的能量和生成物所具有的能量无关 | |
| C. | 化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关 | |
| D. | 由热化学方程式H2(g)+F2(g)═2HF(g)△H=-270 kJ/mol可知2 L氟化氢气体分解成1 L的氢气和1 L的氟气吸收270 kJ热量 |
2.下列实验可达到实验目的是( )
①将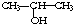 与NaOH的醇溶液共热制备CH3-CH═CH2
与NaOH的醇溶液共热制备CH3-CH═CH2
②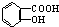 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备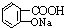
③用浓溴水除去苯中混有的苯酚
④用溴水即可检验CH2=CH-CHO中的碳碳双键.
①将
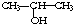 与NaOH的醇溶液共热制备CH3-CH═CH2
与NaOH的醇溶液共热制备CH3-CH═CH2②
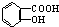 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备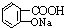
③用浓溴水除去苯中混有的苯酚
④用溴水即可检验CH2=CH-CHO中的碳碳双键.
| A. | 只有①③④ | B. | 只有①④ | C. | 只有① | D. | 都不能 |
1.下列各组物质的最简式相同的是( )
0 152274 152282 152288 152292 152298 152300 152304 152310 152312 152318 152324 152328 152330 152334 152340 152342 152348 152352 152354 152358 152360 152364 152366 152368 152369 152370 152372 152373 152374 152376 152378 152382 152384 152388 152390 152394 152400 152402 152408 152412 152414 152418 152424 152430 152432 152438 152442 152444 152450 152454 152460 152468 203614
| A. | 乙酸和乙二醇 | B. | 乙醚和乙醇 | C. | 甲醛和乙酸 | D. | 乙醛和丙酮 |