20.CCUS是一种二氧化碳的捕获、利用与封存的技术,这种技术可将CO2资源化,产生经济效益.
(1)已知:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1=-820kJ/mol
CO(g)+H2O(g)═CO2(g)+H2(g)△H2=-41.2kJ/mol
2CO(g)+O2(g)═2CO2(g)△H3=-566kJ/mol则反应的
CO2(g)+CH4(g)═2CO(g)+2H2(g)△H=+229.6kJ/mol
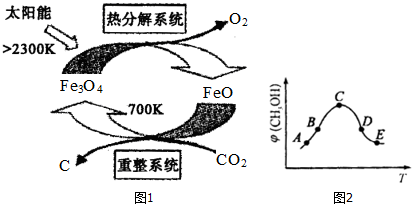
(2)工业上,可利用太阳能以CO2为原料制取C,其原理如图1所示:整个过程中FeO(填“Fe3O4”或“FeO”)是反应的催化剂.重整系统中发生的反应为:6FeO+CO2$\frac{\underline{\;700K\;}}{\;}$2Fe3O4+C每生成1mol Fe3O4,转移电子的物质的量为2mol.
(3)CO2还可用于合成甲醇,反应方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0
①该反应的平衡常数表达式为K=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$.
②在恒容的密闭容器中,加入H2和CO2的混合气体,不同温度条件,反应相同时间后,测得甲醇的体积分数(CH3OH)如图2所示.图中A、B、C、D、E五个点对应的状态中,处于平衡状态的是C、D、E(填字母),B点和E点的反应速率大小关系为v(B)<v(E)(填“>”、“<”、“=”).
③一定温度下,在甲、乙两个容积相同的恒容密闭容器中,加入H2和CO2的混合气体.
甲容器平衡后气体的压强为开始时的80%,要使乙容器达平衡时与甲容器达到相同的平衡状态,且起始时反应逆向进行,则c的取值范围为0.4<n(c)≤1mol.
(1)已知:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1=-820kJ/mol
CO(g)+H2O(g)═CO2(g)+H2(g)△H2=-41.2kJ/mol
2CO(g)+O2(g)═2CO2(g)△H3=-566kJ/mol则反应的
CO2(g)+CH4(g)═2CO(g)+2H2(g)△H=+229.6kJ/mol
(2)工业上,可利用太阳能以CO2为原料制取C,其原理如图1所示:整个过程中FeO(填“Fe3O4”或“FeO”)是反应的催化剂.重整系统中发生的反应为:6FeO+CO2$\frac{\underline{\;700K\;}}{\;}$2Fe3O4+C每生成1mol Fe3O4,转移电子的物质的量为2mol.

(3)CO2还可用于合成甲醇,反应方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0
①该反应的平衡常数表达式为K=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$.
②在恒容的密闭容器中,加入H2和CO2的混合气体,不同温度条件,反应相同时间后,测得甲醇的体积分数(CH3OH)如图2所示.图中A、B、C、D、E五个点对应的状态中,处于平衡状态的是C、D、E(填字母),B点和E点的反应速率大小关系为v(B)<v(E)(填“>”、“<”、“=”).
③一定温度下,在甲、乙两个容积相同的恒容密闭容器中,加入H2和CO2的混合气体.
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、c molCH3OH(g)、c molH2O(g) |
16.利用化学原理对工厂排放的废水、废渣等进行有效检测与合理处理.
(一)染料工业排放的废水中含有大量有毒的NO2-,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体).除去NO2-的离子方程式为2Al+OH-+NO2-+2H2O═2AlO2-+NH3•H2O
(二)某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+):
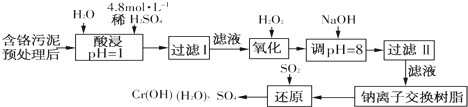
常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)酸浸时,为了提高浸取率可采取的措施是升高温度、搅拌、过滤后再向滤渣中加入硫酸(多次浸取)、适当延长浸取时间(只要答出任意一点即可,其他合理答案也可)(至少写一条).
(2)调pH=8是为了除去Fe3+、Al3+(填Fe3+、Al3+、Ca2+、Mg2+).
(3)钠离子交换树脂的原理为Mn++nNaR→MRn+nNa+,被交换的杂质离子是Mg2+、Ca2+(填Fe3+、Al3+、Ca2+、Mg2+).
(4)试配平氧化还原反应方程式:□Na2Cr2O7+□SO2+□H2O=□Cr(OH)(H2O)5SO4+□Na2SO4;
每生成1mol Cr(OH)(H2O)5SO4消耗SO2的物质的量为1.5mol.
(三)印刷电路铜板腐蚀剂常用FeCl3.腐蚀铜板后的混合浊液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol•L-1,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤:
①通入足量氯气将Fe2+氧化成Fe3+;
②加入CuO调节溶液的pH至3.2~4.7;
③过滤.(提供的药品:Cl2、浓H2SO4、NaOH溶液、CuO、Cu).
0 152227 152235 152241 152245 152251 152253 152257 152263 152265 152271 152277 152281 152283 152287 152293 152295 152301 152305 152307 152311 152313 152317 152319 152321 152322 152323 152325 152326 152327 152329 152331 152335 152337 152341 152343 152347 152353 152355 152361 152365 152367 152371 152377 152383 152385 152391 152395 152397 152403 152407 152413 152421 203614
(一)染料工业排放的废水中含有大量有毒的NO2-,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体).除去NO2-的离子方程式为2Al+OH-+NO2-+2H2O═2AlO2-+NH3•H2O
(二)某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+):

常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀 时的pH | 1.9 | 7.0 | - | - | 4.7 | - |
| 沉淀完全 时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
(2)调pH=8是为了除去Fe3+、Al3+(填Fe3+、Al3+、Ca2+、Mg2+).
(3)钠离子交换树脂的原理为Mn++nNaR→MRn+nNa+,被交换的杂质离子是Mg2+、Ca2+(填Fe3+、Al3+、Ca2+、Mg2+).
(4)试配平氧化还原反应方程式:□Na2Cr2O7+□SO2+□H2O=□Cr(OH)(H2O)5SO4+□Na2SO4;
每生成1mol Cr(OH)(H2O)5SO4消耗SO2的物质的量为1.5mol.
(三)印刷电路铜板腐蚀剂常用FeCl3.腐蚀铜板后的混合浊液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol•L-1,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤:
①通入足量氯气将Fe2+氧化成Fe3+;
②加入CuO调节溶液的pH至3.2~4.7;
③过滤.(提供的药品:Cl2、浓H2SO4、NaOH溶液、CuO、Cu).
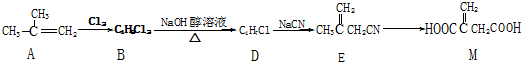
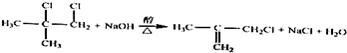
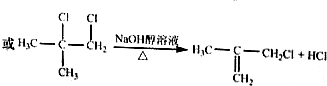 .
. (只写一种)
(只写一种)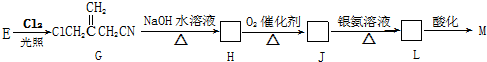
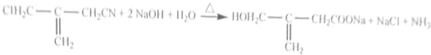
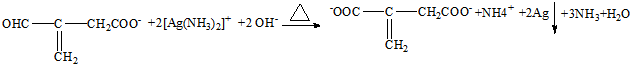
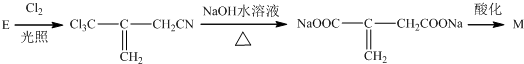 (实例如图1);第二步反应试剂及条件限用NaOH水溶液、加热)
(实例如图1);第二步反应试剂及条件限用NaOH水溶液、加热)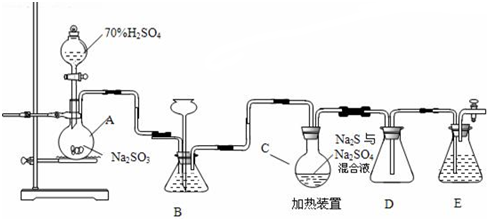
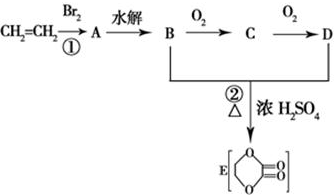
 .
.