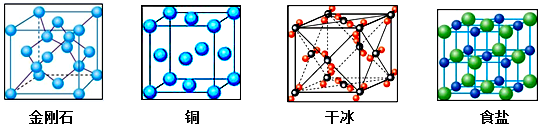
2.下列离子组在指定的溶液中能大量共存的是( )
| A. | 与铝粉反应放出H2的无色溶液:NO3-、Al3+、Na+、SO42- | |
| B. | 使红色石蕊试纸变蓝的溶液:SO42-、HCO3-、K+、Na+ | |
| C. | 中性溶液:Fe3+、Al3+、NO3-、SO42- | |
| D. | 常温下$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:K+、AlO2-、CO32-、Na+、 |
1.设NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 56g金属铁与一定量的硝酸反应时失去的电子数一定为3NA | |
| B. | 2mol SO2和1mol O2在密闭容器中加热(V2O5催化) 充分反应后,容器内分子总数为2NA | |
| C. | 1mol Cu和足量稀硝酸反应产生NA个NO分子 | |
| D. | 常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4NA |
20.设NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 1mol Fe3+完全水解,生成氢氧化铁胶体的数目为NA | |
| B. | 22.4 LCl2 分别与足量的Cu、Fe完全反应转移电子数分别为2 NA、3NA | |
| C. | 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5 NA | |
| D. | 1 mol/L Mg(NO3)2溶液中含有NO3-的数目为2NA |
19.“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是胶体
②是溶液
③能产生丁达尔效应
④能透过滤纸
⑤不能透过滤纸
⑥静置后会析出黑色沉淀.
①是胶体
②是溶液
③能产生丁达尔效应
④能透过滤纸
⑤不能透过滤纸
⑥静置后会析出黑色沉淀.
| A. | ①②⑤ | B. | ①③④ | C. | ②③⑤ | D. | ①③④⑥ |
18.A、B、C、D、E是原子序数依次增大的前四周期的常见元素.已知:
(1)写出E原子基态核外电子排布式1s22s22p63s23p63d104s1.比较B、C、D电负性的大小顺序C<N<O.(按由小到大)
(2)与C2互为等电子体的分子有CO,离子有CN-或C22-.
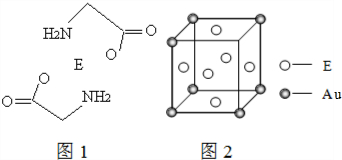
(3)E2+离子与氨基乙酸根离子(H2NCH2COO-)结合得到电中性的配合物(如图1),画出其中E2+离子与N、O原子间的化学键.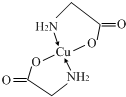 .
.
(4)E和金(Au)形成的合金的晶胞结构如图2,则该合金的化学式可表示为Cu3Au.
| A | 原子半径最小 |
| B | 核外3个能级上的电子数相等 |
| C | 其氢化物的沸点比同族相邻周期元素氢化物的沸点高 |
| D | 2p轨道上成对电子数与未成对电子数相等 |
| E | N层电子数为1,内层轨道全部排满电子 |
(2)与C2互为等电子体的分子有CO,离子有CN-或C22-.
(3)E2+离子与氨基乙酸根离子(H2NCH2COO-)结合得到电中性的配合物(如图1),画出其中E2+离子与N、O原子间的化学键.
 .
.(4)E和金(Au)形成的合金的晶胞结构如图2,则该合金的化学式可表示为Cu3Au.

15.金属锰主要用于高级合金的添加剂.以高铁菱锰矿(主要含MnCO3、FeCO3以及钴、镍等碳酸盐杂质、SiO2等)为原料制取金属锰的工艺流程如下:

下表列出了部分化合物的溶度积常数
(1)写出MnCO3溶浸时反应的化学方程式MnCO3+H2SO4=MnSO4+CO2↑+H2O.滤渣Ⅰ的主要成分为SiO2(填化学式).
(2)写出氧化时反应的离子方程式MnO2+4H+2Fe2+=Mn2++2Fe3++2H2O.
(3)加氨水调节溶液的pH至5.0~6.0,滤渣Ⅱ的主要成分为Fe(OH)3(填化学式),若溶液的pH偏高,将会导致溶液中锰元素的含量降低.
(4)若除杂后,溶液中Co2+、Ni2+的浓度均为1.0×10-5 mol•L-1,则c(S2-)最大=10-17mol•L-1.
(5)电解时阴极电极反应式为Mn2++2e-=Mn.

下表列出了部分化合物的溶度积常数
| 物质 | Fe(OH)3 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 4.0×10-38 | 2.0×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(2)写出氧化时反应的离子方程式MnO2+4H+2Fe2+=Mn2++2Fe3++2H2O.
(3)加氨水调节溶液的pH至5.0~6.0,滤渣Ⅱ的主要成分为Fe(OH)3(填化学式),若溶液的pH偏高,将会导致溶液中锰元素的含量降低.
(4)若除杂后,溶液中Co2+、Ni2+的浓度均为1.0×10-5 mol•L-1,则c(S2-)最大=10-17mol•L-1.
(5)电解时阴极电极反应式为Mn2++2e-=Mn.
14.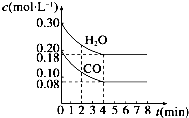 800℃时在体积为1L恒容密闭容器中,通入一定量的CO和H2O(g),发生反应:CO(g)+H2O(g)?H2(g)+CO2(g)CO和H2O(g)浓度变化如图所示.下列说法正确的是( )
800℃时在体积为1L恒容密闭容器中,通入一定量的CO和H2O(g),发生反应:CO(g)+H2O(g)?H2(g)+CO2(g)CO和H2O(g)浓度变化如图所示.下列说法正确的是( )
 800℃时在体积为1L恒容密闭容器中,通入一定量的CO和H2O(g),发生反应:CO(g)+H2O(g)?H2(g)+CO2(g)CO和H2O(g)浓度变化如图所示.下列说法正确的是( )
800℃时在体积为1L恒容密闭容器中,通入一定量的CO和H2O(g),发生反应:CO(g)+H2O(g)?H2(g)+CO2(g)CO和H2O(g)浓度变化如图所示.下列说法正确的是( )| A. | 容器中气体的压强不再改变则反应达到平衡 | |
| B. | 4 min后升高温度,CO和H2O(g)浓度也升高,则△H<0 | |
| C. | 800℃时只改变CO和H2O(g)起始投料,分别达平衡,CO的转化率与H2O(g)的转化率之和不变 | |
| D. | 若起始充入0.30mol CO、0.10mol H2O、0.20mol CO2和20mol H2,则反应将向正反应方向进行 |
13.下列有关实验原理、方法或结论的描述正确的是( )
0 152203 152211 152217 152221 152227 152229 152233 152239 152241 152247 152253 152257 152259 152263 152269 152271 152277 152281 152283 152287 152289 152293 152295 152297 152298 152299 152301 152302 152303 152305 152307 152311 152313 152317 152319 152323 152329 152331 152337 152341 152343 152347 152353 152359 152361 152367 152371 152373 152379 152383 152389 152397 203614
| A. | 配制FeSO4溶液时,需加入少量铁粉和稀盐酸,既防止氧化又抑制水解 | |
| B. | 向纯水中加入盐酸或降温都能使电离平衡逆向移动,但水的离子积不变 | |
| C. | 在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,验证Na2CO3溶液中存在水解平衡 | |
| D. | 已知I3-?I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |