题目内容
20.设NA为阿伏伽德罗常数,下列叙述正确的是( )| A. | 1mol Fe3+完全水解,生成氢氧化铁胶体的数目为NA | |
| B. | 22.4 LCl2 分别与足量的Cu、Fe完全反应转移电子数分别为2 NA、3NA | |
| C. | 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5 NA | |
| D. | 1 mol/L Mg(NO3)2溶液中含有NO3-的数目为2NA |
分析 A、一个氢氧化铁胶粒是多个氢氧化铁的聚集体;
B、氯气的状态不明确;
C、乙烯和丁烯的最简式均为CH2;
D、溶液体积不明确.
解答 解:A、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故形成的氢氧化铁胶粒个数小于NA个,故A错误;
B、氯气的状态不明确,故其物质的量无法计算,则转移的电子数无法计算,故B错误;
C、乙烯和丁烯的最简式均为CH2,故21g混合物中含有的CH2的物质的量为1.5mol,则含1.5mol碳原子即1.5NA个,故C正确;
D、溶液体积不明确,故溶液中的硝酸根的个数无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列设计的实验方案能达到实验目的是( )
| A. | 制备Al(OH)3悬浊液:向1mol•L-1AlCl3溶液中加过量的6mol•L-1NaOH溶液 | |
| B. | 提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量饱和碳酸钠溶液,振荡后静置分液,并除去有机相的水 | |
| C. | 检验溶液中是否含有Fe3+:取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,观察实验现象 | |
| D. | 探究催化剂对H2O2分解速率的影响:在相同条件下,向一试管中加入2mL5%H2O2和1mLH2O,向另一试管中加入2mL 10%H2O2和1mLFeCl3溶液,观察并比较实验现象 |
11.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 1mol H2O含有的原子数为NA | |
| B. | 4gH2含有氢分子数4NA | |
| C. | 常温常压下,11.2L O2中含有分子数为0.5NA | |
| D. | 1L 0.1 mol•L-1NaCl溶液中含Na+数0.1NA |
8.用下列实验仪器或装置进行相应实验,能达到实验目的是( )
| A. |  实验测定氯水的pH | |
| B. | 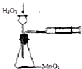 实验定量测定H2O2的分解速率 | |
| C. | 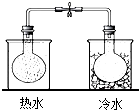 实验中利用NO2颜色的变化验证其中反应的热效应 | |
| D. | 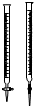 实验中(乙)管内盛放已知浓度的KMnO4溶液来测定FeSO4溶液的浓度 |
15.金属锰主要用于高级合金的添加剂.以高铁菱锰矿(主要含MnCO3、FeCO3以及钴、镍等碳酸盐杂质、SiO2等)为原料制取金属锰的工艺流程如下:

下表列出了部分化合物的溶度积常数
(1)写出MnCO3溶浸时反应的化学方程式MnCO3+H2SO4=MnSO4+CO2↑+H2O.滤渣Ⅰ的主要成分为SiO2(填化学式).
(2)写出氧化时反应的离子方程式MnO2+4H+2Fe2+=Mn2++2Fe3++2H2O.
(3)加氨水调节溶液的pH至5.0~6.0,滤渣Ⅱ的主要成分为Fe(OH)3(填化学式),若溶液的pH偏高,将会导致溶液中锰元素的含量降低.
(4)若除杂后,溶液中Co2+、Ni2+的浓度均为1.0×10-5 mol•L-1,则c(S2-)最大=10-17mol•L-1.
(5)电解时阴极电极反应式为Mn2++2e-=Mn.

下表列出了部分化合物的溶度积常数
| 物质 | Fe(OH)3 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 4.0×10-38 | 2.0×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(2)写出氧化时反应的离子方程式MnO2+4H+2Fe2+=Mn2++2Fe3++2H2O.
(3)加氨水调节溶液的pH至5.0~6.0,滤渣Ⅱ的主要成分为Fe(OH)3(填化学式),若溶液的pH偏高,将会导致溶液中锰元素的含量降低.
(4)若除杂后,溶液中Co2+、Ni2+的浓度均为1.0×10-5 mol•L-1,则c(S2-)最大=10-17mol•L-1.
(5)电解时阴极电极反应式为Mn2++2e-=Mn.
5.含8.0g NaOH 的溶液中通入一定量CO2后,将得到的溶液低温小心蒸干,称得无水物9.3g,则该无水物中一定含有的物质是( )
| A. | Na2CO3 | B. | NaHCO3 | C. | Na2CO3 和NaHCO3 | D. | NaOH和Na2CO3 |
12.下列溶液中氯离子浓度最小的是( )
| A. | 150ml 1mol/L的NaCl溶液 | B. | 150ml 3mol/LKCl溶液 | ||
| C. | 75ml 2mol/L的NH4Cl溶液 | D. | 50ml 1mol/lCuCl2溶液 |
9.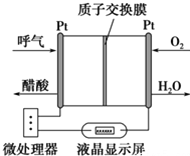 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )| A. | 该电池的负极反应式为:CH3CH2OH+3H2O-12e-═2CO2↑+12H+ | |
| B. | 该电池的正极反应式为:O2+4e-+4H+═2H2O | |
| C. | 电流由O2所在的铂电极经外电路流向另一电极 | |
| D. | 微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
10.将海水淡化和与浓海水资源化结合起来是综合利用海水的重要途径之一.一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺提取其他产品.回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是②③④(填序号).
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾.溴.镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收.碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为$\frac{5}{3}$mol.
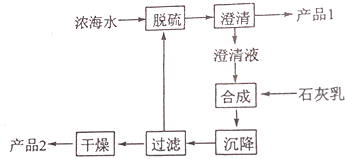
(3)海水提镁的一段工艺流程如图:浓海水的主要成分如下:
该工艺过程中,脱硫阶段主要反应的离子方程式为Ca2++SO42-=CaSO4↓,产品2的化学式为Mg(OH)2,1L浓海水最多可得到产品2的质量为69.6g.
(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式Mg+2H2O$\frac{\underline{\;高温\;}}{\;}$Mg(OH)2+H2↑.

(1)下列改进和优化海水综合利用工艺的设想和做法可行的是②③④(填序号).
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾.溴.镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收.碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为$\frac{5}{3}$mol.
(3)海水提镁的一段工艺流程如图:浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式Mg+2H2O$\frac{\underline{\;高温\;}}{\;}$Mg(OH)2+H2↑.