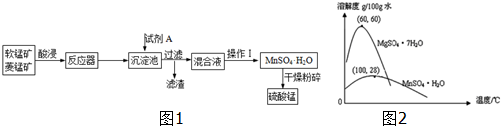
5.硫酸锰可用于饲料营养强氧化剂和媒染剂.其生产原材料软锰矿(MnO2)、菱锰矿(MnCO3)中常混有硫酸亚铁和硫酸镁等杂质,生产工艺如图1:
已知:(1)硫酸锰晶体和硫酸镁晶体的溶解度曲线如图2.(2)完全沉淀离子的pH:Fe3+为3.5,Fe2+为9.5,Mn2+为10.8,Mg2+为l1.6.
下列判断正确的是( )
已知:(1)硫酸锰晶体和硫酸镁晶体的溶解度曲线如图2.(2)完全沉淀离子的pH:Fe3+为3.5,Fe2+为9.5,Mn2+为10.8,Mg2+为l1.6.
下列判断正确的是( )

| A. | 试剂A应该选择H2O2,目的是将Fe2+氧化为Fe3+ | |
| B. | 试剂A应该选择氨水,目的是调节溶液的pH | |
| C. | 操作I包括蒸发、冷却、结晶、趁热过滤、洗涤、等步骤,洗涤时可用稀硫酸做洗液 | |
| D. | 在蒸发结晶时,温度应该高于60°C |
4.天津“8.12“爆炸中扩散的CN-造成部分水体污染.某小组欲检测污水中CN-的浓度并模拟电化学法除去CN-.
探究I 检测CN-浓度
资料:碱性条件下发生离子反应:2CN-+5H202+90H-═2CO32-+N2+6H20
实验装置如图1(其中加热、夹持装置省略).(不考虑污水中其它离子反应)
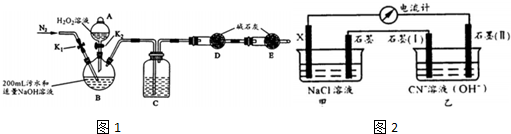
(1)加入药品之前的操作是检查装置气密性;C中试剂是浓H2S04
(2)实验步骤如下:
(3)计算CN-的浓度,需称得的质量是反应前后D装置的质量.
(4)为了使检测更加准确,上述(2)中操作要特别注意一些事项.请写出至少一条加稀H2S04时要缓慢注入(要缓慢通人N2或给B加热时温度不能过高或加入稀H2SO4,要足量).
探究Ⅱ电化学法处理CN-的影响因素由如图2装置模拟电化学法实验,有关结果如表.
(5)根据表格信息分析.
①X电极名称:负极;
②实验(1)中X换成Zn,则电流计读数的范围为I~1.5I
③若乙装置中阳极产生无毒无害物质,其电极方程式为2CN-+12OH--10e-=2CO32-+N2+6H2O;该实验说明电化学法处理CN-,影响处理速率的因素有负极的金属材料和甲中电解质的浓度(至少两条).
探究I 检测CN-浓度
资料:碱性条件下发生离子反应:2CN-+5H202+90H-═2CO32-+N2+6H20
实验装置如图1(其中加热、夹持装置省略).(不考虑污水中其它离子反应)

(1)加入药品之前的操作是检查装置气密性;C中试剂是浓H2S04
(2)实验步骤如下:
| 步骤1 | 关闭K1,打开K2,滴入足量H2O2溶液,对B加热.充分反应后,停止加热 |
| 步骤2 | 关闭K2,用注射器穿过B装置的胶塞注入 稀H2S04溶液 |
| 步骤3 | 打开K1,通入N2 |
(4)为了使检测更加准确,上述(2)中操作要特别注意一些事项.请写出至少一条加稀H2S04时要缓慢注入(要缓慢通人N2或给B加热时温度不能过高或加入稀H2SO4,要足量).
探究Ⅱ电化学法处理CN-的影响因素由如图2装置模拟电化学法实验,有关结果如表.
| 实验序号 | 电极(X) | NaCl溶液浓度 (mol/L) | 甲中石墨表面通入气体 | 电流计读数 (A) |
| (1) | Fe | 0.1 | 空气 | I |
| (2) | Al | 0.1 | 空气 | 1.5I |
| (3) | Fe | 0.1 | O2 | 2I |
| (4) | Al | 0.5 | 空气 | 1.6I |
①X电极名称:负极;
②实验(1)中X换成Zn,则电流计读数的范围为I~1.5I
③若乙装置中阳极产生无毒无害物质,其电极方程式为2CN-+12OH--10e-=2CO32-+N2+6H2O;该实验说明电化学法处理CN-,影响处理速率的因素有负极的金属材料和甲中电解质的浓度(至少两条).
2.资料显示:a.Na2S2O3、BaS2O3、BaS均易溶于水.b.SO2、Na2S、Na2CO3反应可生成Na2S2O3.某化学小组据此进行了制备硫代硫酸钠(Na2S2O3)的探究:实验制备装置如图所示(省略夹持装置):

回答问题:
(1)仪器a的名称是分液漏斗.
(2)装置B中的长颈漏斗的作用是平衡压强
(3)在装置C中生成Na2S2O3.
①完成反应方程式:4SO2+2Na2S+1Na2CO3=3Na2S2O3+□
②反应开始先使A中发生反应一会儿,再使C中反应发生,其原因是排除装置内空气,防止发生氧化生成Na2SO4.
(4)完成对所得产品的检测的实验:

回答问题:
(1)仪器a的名称是分液漏斗.
(2)装置B中的长颈漏斗的作用是平衡压强
(3)在装置C中生成Na2S2O3.
①完成反应方程式:4SO2+2Na2S+1Na2CO3=3Na2S2O3+□
②反应开始先使A中发生反应一会儿,再使C中反应发生,其原因是排除装置内空气,防止发生氧化生成Na2SO4.
(4)完成对所得产品的检测的实验:
| 推测 | 操作和现象 | 结论 |
| 杂质中的正盐成分可能有: A,、Na2S B,、Na2CO3 C,、Na2SO4 D,、Na2SO3 | ①取Wg产品配成稀溶液; ②向溶液中滴加过量BaCl2溶液,有白色沉淀生成,过滤,得沉淀和滤液; ③向沉淀中加入过量盐酸,沉淀完全溶解,并有刺激性气味的气体产生. ④向滤液滴加2滴淀粉溶液,再逐滴加0.1000mol•L-1碘的标准溶液,消耗碘的标准溶液体积为18.10mL. | 产品杂质中: 一定含有Na2SO3, 可能含有Na2CO3Na2S, 一定不含有Na2SO4. 操作④发生的反应是: 2S2O32-+I2═S4O${\;}_{6}^{2-}$+2I- Ⅰ、判断达到滴定终点的现象是溶液由无色变蓝色,且半分钟不褪色 Ⅱ、产品纯度:(9/W)×100%. |
1.下列说法正确的是( )
| A. | 钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水 | |
| B. | Na2O的水溶液能导电,不能说明Na2O是电解质 | |
| C. | 石英和玛瑙的主要成分均为二氧化硅,其分子式为SiO2 | |
| D. | 酸性氧化物大多数是非金属氧化物,因此不能与酸溶液发生反应 |
20. X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如表:
X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如表:
(1)Y在元素周期表中的位置是第三周期ⅢA族.
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是O2- (填离子符号).
(3)Q和R按原子个数比1:1组成的化合物甲,是一种“绿色”氧化剂.
①甲的电子式是 .
.
②空气阴极法电解制备甲的装置如图所示.在碱性溶液中,将空气中的氧气还原得到甲和稀碱的溶液,则图中直流电源的a是正极.
 X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如表:
X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如表:| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是O2- (填离子符号).
(3)Q和R按原子个数比1:1组成的化合物甲,是一种“绿色”氧化剂.
①甲的电子式是
 .
.②空气阴极法电解制备甲的装置如图所示.在碱性溶液中,将空气中的氧气还原得到甲和稀碱的溶液,则图中直流电源的a是正极.
19.实验室中需要0.2mol•L-1的CuSO4溶液950mL,配制时应选用的容量瓶的规格和称取胆矾晶体(CuSO4•5H2O式量为250)的质量分别是( )
| A. | 1000mL 50.0g | B. | 950mL 47.5g | C. | 950mL 30.4g | D. | 1000mL 32.0g |
18.下列事实中,能用同一化学原理解释的是( )
| A. | 氯气和二氧化硫都能使品红溶液褪色 | |
| B. | 异戊烷和异戊二烯都能使溴水层褪色 | |
| C. | 亚硫酸钠和乙烯都能使酸性高锰酸钾溶液褪色 | |
| D. | 活性炭与氢氧化钠溶液都能使二氧化氮气体褪色 |
17.下列有关颜色变化的叙述不正确的是 ( )
0 152147 152155 152161 152165 152171 152173 152177 152183 152185 152191 152197 152201 152203 152207 152213 152215 152221 152225 152227 152231 152233 152237 152239 152241 152242 152243 152245 152246 152247 152249 152251 152255 152257 152261 152263 152267 152273 152275 152281 152285 152287 152291 152297 152303 152305 152311 152315 152317 152323 152327 152333 152341 203614
| A. | 淀粉溶液中滴入碘水--变蓝色 | B. | 溴化银见光分解--变黑色 | ||
| C. | 苯酚溶液中滴入Fe 3+--变紫色 | D. | 胆矾空气中久置--变白色 |
