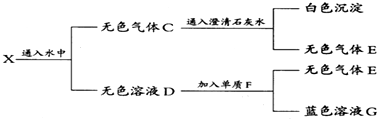
9.下列关于氨水的叙述正确的是( )
| A. | 氨水显碱性,是因为氨水是一种弱碱 | |
| B. | 氨水和液氨成分相同 | |
| C. | 氨水中物质的量浓度最大的粒子是NH3•H2O(除水外) | |
| D. | 氨水中共有五种粒子 |
8.下列各醇中,能发生消去反应生成(CH3)2C═CH2的是( )
| A. | CH3-OH | B. |  | C. | C2H5OH | D. |  |
7.对下列气体进行“喷泉”实验,在干燥的烧瓶中分别装入下列气体,打开止水夹,形成喷泉,其中溶液不能充满烧瓶的是( )
| A. | NH3 | B. | NO2 | ||
| C. | HCl | D. | 体积比为4:1的NO2和O2的混合气体 |
6.某无色透明溶液与金属铁反应时只放出氢气,则溶液中可以大量共存的离子是( )
| A. | Na+、S2-、H+、SO42- | B. | H+、NO3-、Ba2+、Mg2+ | ||
| C. | Na+、Cl-、H+、SO42- | D. | Ba2+、K+、CO32-、OH- |
3.下列溶液中,能用来区别SO2和CO2气体的是( )
①石灰水 ②H2S溶液 ③KMnO4溶液 ④紫色石蕊溶液 ⑤BaCl2溶液 ⑥品红溶液.
①石灰水 ②H2S溶液 ③KMnO4溶液 ④紫色石蕊溶液 ⑤BaCl2溶液 ⑥品红溶液.
| A. | ①④⑤ | B. | ②④⑤ | C. | ③④⑤ | D. | ②③⑥ |
2. 如图是实验室制备1,2-二溴乙烷并进行一系列相关实验的装置(加热及夹持设备已略).
如图是实验室制备1,2-二溴乙烷并进行一系列相关实验的装置(加热及夹持设备已略).
有关数据列表如下:
(1)A中药品为1:3的无水乙醇和浓硫酸混合液,使用连通滴液漏斗相比使用分液漏斗滴加液体的优点是能使连通滴液漏斗里的溶液容易滴下;B中插长玻璃管的作用有:稳压作用,可检查装置是否发生堵塞.
(2)写出C装置中的离子反应方程式SO2+2OH-=SO32-+H2O、CO2+2OH-=CO32-+H2O;装置D中品红溶液的作用是验证二氧化硫是否被除尽.
(3)反应过程中应用冷水冷却装置E,其主要目的是减少液溴挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷易凝结成固体而发生堵塞.
(4)学生发现反应结束时,无水乙醇消耗量大大超过理论值,其原因是乙醇挥发、副反应发生或反应太剧烈.
(5)装置F的作用是吸收挥发出的溴蒸汽,减少对环境的污染;写出F装置中发生反应的化学方程式Br2+2NaOH=NaBr+NaBrO+H2O.
0 152055 152063 152069 152073 152079 152081 152085 152091 152093 152099 152105 152109 152111 152115 152121 152123 152129 152133 152135 152139 152141 152145 152147 152149 152150 152151 152153 152154 152155 152157 152159 152163 152165 152169 152171 152175 152181 152183 152189 152193 152195 152199 152205 152211 152213 152219 152223 152225 152231 152235 152241 152249 203614
 如图是实验室制备1,2-二溴乙烷并进行一系列相关实验的装置(加热及夹持设备已略).
如图是实验室制备1,2-二溴乙烷并进行一系列相关实验的装置(加热及夹持设备已略).有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(2)写出C装置中的离子反应方程式SO2+2OH-=SO32-+H2O、CO2+2OH-=CO32-+H2O;装置D中品红溶液的作用是验证二氧化硫是否被除尽.
(3)反应过程中应用冷水冷却装置E,其主要目的是减少液溴挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷易凝结成固体而发生堵塞.
(4)学生发现反应结束时,无水乙醇消耗量大大超过理论值,其原因是乙醇挥发、副反应发生或反应太剧烈.
(5)装置F的作用是吸收挥发出的溴蒸汽,减少对环境的污染;写出F装置中发生反应的化学方程式Br2+2NaOH=NaBr+NaBrO+H2O.