9.下列物质中既能与稀硫酸反应,又能与NaOH溶液反应的是( )
①NaHCO3 ②Al(OH)3 ③NH4HSO3 ④Al2O3 ⑤Al.
①NaHCO3 ②Al(OH)3 ③NH4HSO3 ④Al2O3 ⑤Al.
| A. | ②④⑤ | B. | ①②④⑤ | C. | ②③④⑤ | D. | 全部 |
8.下列有机物中,含有两种官能团的是( )
| A. | CH3-CH2-Cl | B. | CH3CHO | C. | CH2=CHBr | D. | CH3CH3-OH |
7.设NA为阿伏加德罗常数的值,下列有关说法正确的是( )
| A. | 常温常压下,17g甲基(-14CH3)所含的中子数为9NA | |
| B. | 1mol/L的Mg(NO3)2溶液中含有的NO3-的数目为2 NA | |
| C. | 铁与0.1mol氯气在点燃条件下充分反应,转移的电子数为0.3NA | |
| D. | 42.0 g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
6.下列方程式不正确的是( )
| A. | 向NaHCO3溶液中加入过量的石灰水产生白色沉淀:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 向AgCl悬浊液中滴加Na2S溶液产生黑色沉淀:2AgCl(s)+S2-═Ag2S(s)+2Cl- | |
| C. | 石灰乳中Ca(OH)2的电离:Ca(OH)2(s)═Ca2++2OH- | |
| D. | Fe(OH)3胶体的制备:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl |
2.下列化学方程式能用H++OH-═H2O表示的是( )
| A. | 硫酸和氢氧化钡 | B. | 氢氧化铜和盐酸 | C. | 盐酸和氨水 | D. | 氢氧化钠和硫酸 |
1.下列叙述中正确的是( )
| A. | 电离时能够产生H+的化合物是酸 | |
| B. | 难溶的物质(如CaCO3)不能发生离子反应 | |
| C. | 电解质在水中不一定能导电,在水中导电的化合物不一定是电解质 | |
| D. | 胶体加入电解质可产生沉淀,而溶液不能 |
20.科学家指出,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒,这是因为对人体无害的+5价砷类物质在维生素C的作用下,能够转化为有毒的+3价砷类化合物.下列说法不正确的是( )
0 152047 152055 152061 152065 152071 152073 152077 152083 152085 152091 152097 152101 152103 152107 152113 152115 152121 152125 152127 152131 152133 152137 152139 152141 152142 152143 152145 152146 152147 152149 152151 152155 152157 152161 152163 152167 152173 152175 152181 152185 152187 152191 152197 152203 152205 152211 152215 152217 152223 152227 152233 152241 203614
| A. | 维生素C具有还原性 | |
| B. | 上述过程中砷元素发生还原反应 | |
| C. | 上述过程中+5价砷类物质作氧化剂 | |
| D. | 上述过程中+3价砷类化合物是氧化产物 |
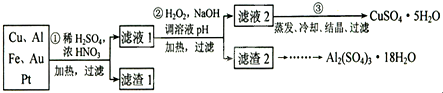
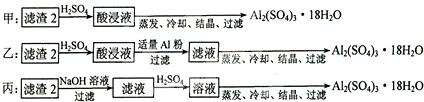
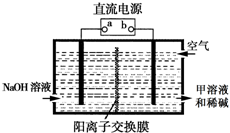 X、Y、Z、Q、R是五种短周期元素,原子序数依次增大.X元素一种原子核无中子.Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素.
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大.X元素一种原子核无中子.Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素.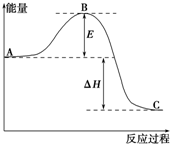 2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.请回答下列问题:
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.请回答下列问题: