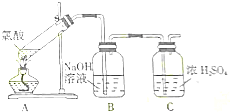
19.下列诸因素中,可以解释水的熔、沸点比氯化钠低的是( )
| A. | 水分子中共价键比氯化钠中离子键弱 | |
| B. | 水的相对分子质量比氯化钠的小 | |
| C. | 水分子间有范德华力,氯化钠分子间的作用力较强 | |
| D. | 水分子间是以范德华力相结合,相互作用较弱;氯化钠晶体中,Na+和Cl-以离子键相结合,作用力较强 |
18.分子式为C4H8O的单官能团化合物中,属于链状结构的物质有( )种.(不考虑立体异构)
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
17.有4种混合溶液,分别由等体积等物质的量浓度的2种溶液混合而成,①NH4Cl与HCl;②NH4Cl与NaOH;③NH4Cl与NaCl;④NH4Cl与AlCl3,下列说法正确的是( )
| A. | c(NH4+):②>④>③>① | B. | pH:②>③>④>① | ||
| C. | c(H+):①>③>②>④ | D. | c(NH3•H2O):②>④>③>① |
16.可用于鉴别氧化铜、铁粉、炭粉、二氧化锰四种黑色粉末(必要时可加热)的试剂是( )
| A. | 水 | B. | 氢氧化钠溶液 | C. | 浓盐酸 | D. | 氯化铁溶液 |
15.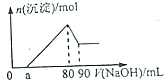 Fe2O3和Al2O3的混合物完全溶解于160mL2mol/LHCl溶液中,在所得溶液中滴加NaOH溶液得到如图,下列说法不正确的是( )
Fe2O3和Al2O3的混合物完全溶解于160mL2mol/LHCl溶液中,在所得溶液中滴加NaOH溶液得到如图,下列说法不正确的是( )
 Fe2O3和Al2O3的混合物完全溶解于160mL2mol/LHCl溶液中,在所得溶液中滴加NaOH溶液得到如图,下列说法不正确的是( )
Fe2O3和Al2O3的混合物完全溶解于160mL2mol/LHCl溶液中,在所得溶液中滴加NaOH溶液得到如图,下列说法不正确的是( )| A. | 若a=20mL时,则混合物中Fe2O3占0.02mol | |
| B. | 所滴加的Na0H溶液的浓度为4mol/L | |
| C. | a点处,Na0H溶液的体积为a<50mL | |
| D. | 若a=20mL,则剩余盐酸的体积为20mL |
13.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1L1mol/L的碳酸钠溶液中含CO32-NA个 | |
| B. | 标准状况下,11.2L甲醇与足量钠反应,可生成标准状况下氢气5.6L | |
| C. | H2O2和H2O的混合物1mol中,含阴离子个数为NA | |
| D. | 标准状况下,22.4LCl2与足量铁充分反应,电子转移数为2NA |
11.某实验小组按如表中的装置进行实验,已知电极A、B、C、D分别是Mg、Al、Cu、Ag中的一种,
根据实验现象回答下列问题:
(1)A、D分别为Al、Cu.
(2)乙装置中C电极的电极反应式为2H2O+2e-═H2↑+2OH-.
(3)上述实验证明了“利用金属活动性顺序可直接判断原电池的正负极”,这种做法不可靠(填“可靠”或“不可靠”)
0 151973 151981 151987 151991 151997 151999 152003 152009 152011 152017 152023 152027 152029 152033 152039 152041 152047 152051 152053 152057 152059 152063 152065 152067 152068 152069 152071 152072 152073 152075 152077 152081 152083 152087 152089 152093 152099 152101 152107 152111 152113 152117 152123 152129 152131 152137 152141 152143 152149 152153 152159 152167 203614
| 装置 | 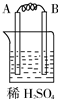 甲 甲 | 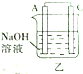 | 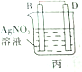 | 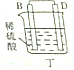 |
| 现象 | A不断溶解 | A极有气泡产生 | B电极质量增加 | B、D电极均无明显变化 |
(1)A、D分别为Al、Cu.
(2)乙装置中C电极的电极反应式为2H2O+2e-═H2↑+2OH-.
(3)上述实验证明了“利用金属活动性顺序可直接判断原电池的正负极”,这种做法不可靠(填“可靠”或“不可靠”)