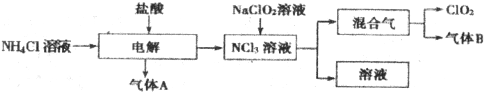
题目内容
12.(1)我国是以煤炭为主要燃料的国家,在煤中加入石灰石可有效减少SO2排放,即所谓“钙基固硫“最后在煤渣中生成硫酸钙,两步反应化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑、2CaO+2S+3O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4(2)为了SO2的再利用和防止这种污染,硫酸厂可用氨水吸收SO2生成亚硫酸铵[(NH4)2SO3],再用硫酸处理,可回收SO2并得到化肥硫酸按[(NH4)2SO4],两步反应的离子方程式为:SO2+2NH3.H2O=2NH4++SO32-、SO32-+2H+=SO2↑+H2O.
分析 (1)高温条件下石灰石分解生成CaO,S和CaO、O2反应生成硫酸钙;
(2)二氧化硫属于酸性氧化物,能和弱碱氨水反应生成亚硫酸铵[(NH4)2SO3],强酸能和弱酸盐反应生成弱酸.
解答 解:(1)高温条件下石灰石分解生成CaO,S和CaO、O2反应生成硫酸钙,从而降低二氧化硫的排放,减少污染,两步反应化学方程式分别为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑、2CaO+2S+3O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4,
故答案为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;2CaO+2S+3O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4;
(2)二氧化硫属于酸性氧化物,能和弱碱氨水反应生成亚硫酸铵[(NH4)2SO3],强酸能和弱酸盐反应生成弱酸,两步离子方程式分别为SO2+2NH3.H2O=2NH4++SO32-、SO32-+2H+=SO2↑+H2O,
故答案为:SO2+2NH3.H2O=2NH4++SO32-;SO32-+2H+=SO2↑+H2O.
点评 本题考查化学方程式、离子方程式的书写,为高频考点,明确反应物、生成物及反应条件、离子方程式书写规则即可解答,注意:弱电解质在离子方程式中要写化学式.

练习册系列答案
相关题目
2.关于如图所示转化关系(X代表卤族元素)说法正确的是( )
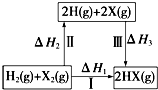

| A. | H2(g)+X2(g)═2H(g)+2X(g)△H2<0 | |
| B. | △H1=△H2+△H3 | |
| C. | 途径Ⅲ的按Cl、Br、I顺序依次增大 | |
| D. | 途径Ⅰ生成HCl比生成HBr的△H1小,说明HCl比HBr稳定 |
3.下列关于浓硫酸叙述正确的是( )
| A. | 浓硫酸能使湿润的蓝色石蕊试纸先变红后变黑 | |
| B. | 浓硫酸在常温下可迅速与铜片反应,放出二氧化硫气体 | |
| C. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 | |
| D. | 浓硫酸在常温下能使铁铝等金属钝化,加热条件下也不反应 |
20.NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 37gNH4F和16gCH4中含有的共价键数均为4NA | |
| B. | 0.51.4mol•L-1的NaHSO3溶液中含有的SO32-数为2NA | |
| C. | 标准状况下,16.8LNO2完全溶于水,转移电子数为0.5NA | |
| D. | 高温高压和催化剂条件下,密闭容器中2gH2与足量N2反应,转移电子数为2NA |
17.有4种混合溶液,分别由等体积等物质的量浓度的2种溶液混合而成,①NH4Cl与HCl;②NH4Cl与NaOH;③NH4Cl与NaCl;④NH4Cl与AlCl3,下列说法正确的是( )
| A. | c(NH4+):②>④>③>① | B. | pH:②>③>④>① | ||
| C. | c(H+):①>③>②>④ | D. | c(NH3•H2O):②>④>③>① |
1.纯水在95℃和25℃时的pH( )
| A. | 前者大 | B. | 后者大 | C. | 相等 | D. | 无法确定 |