8.下列各方程式中,属于水解反应的是( )
| A. | CO2+H2O?H2CO3 | B. | OH-+HS-?S2-+H2O | ||
| C. | HS-+H2O?H3O++S2- | D. | S2-+H2?HS-+OH- |
7.NaCl是一种化工原料,可以制备一系列物质(见图).下列说法正确的是( )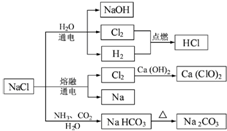

| A. | 25℃,NaHCO3在水中的溶解度比Na2CO3的大 | |
| B. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| C. | 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 图中所示转化反应不都是氧化还原反应 |
6.下列离子方程式中正确的是( )
| A. | H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | CH3COOH溶液与NaOH溶液反应:H++OH-═H2O | |
| C. | 铁与稀硫酸反应:Fe+2H+═Fe2++H2↑ | |
| D. | 硫酸与Cu(OH)2反应:H++OH-═H2O |
5.下列各组离子,能在溶液中大量共存的是( )
| A. | Na+、Mg2+、Cl-、OH- | B. | H+、Ca2+、CO32-、NO3- | ||
| C. | Cu2+、K+、SO42-、NO3- | D. | Na+、HCO3-、K+、H+ |
4.下列关于胶体的说法正确的是( )
| A. | 利用布朗运动可区别溶液和胶体 | |
| B. | 溶液中通过一束光线时没有明显现象,胶体中通过一束光线时出现明显的光路 | |
| C. | 胶体微粒带电荷,溶液中溶质微粒不带电荷 | |
| D. | 制备Fe(OH)3胶体的方法是:将饱和FeCl3溶液通入热的NaOH溶液中并持续煮沸 |
3.下列说法正确的是( )
| A. | 常温下,反应C(s)+H2O(g)═CO(g)+H2(g)不能自发进行,则该反应的△H>0 | |
| B. | 一定温度下,反应MgCl2(l)═Mg(l)+Cl2(g)的△H>0,△S<0 | |
| C. | 放热的自发过程,一定是熵增加的过程 | |
| D. | 液态水可自发挥发成水蒸气的过程是熵减的过程 |
1.下列分离方法中,正确的是( )
| A. | 将碘晶体中含有的少量沙子除去采用蒸馏的方法 | |
| B. | 蒸馏操作使用的温度计的水银球应插入到液体内 | |
| C. | 分离液体时,分液漏斗上的小孔与大气相通时打开活塞 | |
| D. | 若分液时不小心有少量上层液体流下来,补救措施是用滴管将其从烧杯中吸出 |
20.氮元素能形成多种多样的化合物.
(1)己知N2O4(g)═2NO2(g)△H=+57.20kJ/mol,t℃时,将一定量的NO2、N2O4,充人一个容器为2L的恒容密闭容器中,浓度随时间变化关系如表所示:
①c(X)代表NO2(填化学式)的浓度,该反应的平衡常数K=0.9.
②20min时改变的条件是增大二氧化氮浓度;重新达到平衡时,NO2的转化率将b(填选项前字母).
a.增大 b.减小 c.不变 d.无法判断
③t℃时,下列情况不能说明该反应处于平衡状态的是A;
A.混合气体的密度保持不变 B.混合气体的颜色不再变化
C.混合气体的气体压强保持不变 D.N2O4 与NO2的物质的量比为10:3
④若反应在t℃进行,某时刻测得n(NO2)=0.6mol、n(N2O4)=1.2mol,则此时v(正)>v(逆)(填“>”、“<”或“=”).
(2)已知2N2H4(l)+N2O4(l)═3N2(g)+4H2O(l)△H=-1225kJ/mol
则使1mol N2O4(l)完全分解成相应的原子时需要吸收的能量是1793kJ.
0 151851 151859 151865 151869 151875 151877 151881 151887 151889 151895 151901 151905 151907 151911 151917 151919 151925 151929 151931 151935 151937 151941 151943 151945 151946 151947 151949 151950 151951 151953 151955 151959 151961 151965 151967 151971 151977 151979 151985 151989 151991 151995 152001 152007 152009 152015 152019 152021 152027 152031 152037 152045 203614
(1)己知N2O4(g)═2NO2(g)△H=+57.20kJ/mol,t℃时,将一定量的NO2、N2O4,充人一个容器为2L的恒容密闭容器中,浓度随时间变化关系如表所示:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/(mol/L) | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(Y)/(mol/L) | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
②20min时改变的条件是增大二氧化氮浓度;重新达到平衡时,NO2的转化率将b(填选项前字母).
a.增大 b.减小 c.不变 d.无法判断
③t℃时,下列情况不能说明该反应处于平衡状态的是A;
A.混合气体的密度保持不变 B.混合气体的颜色不再变化
C.混合气体的气体压强保持不变 D.N2O4 与NO2的物质的量比为10:3
④若反应在t℃进行,某时刻测得n(NO2)=0.6mol、n(N2O4)=1.2mol,则此时v(正)>v(逆)(填“>”、“<”或“=”).
(2)已知2N2H4(l)+N2O4(l)═3N2(g)+4H2O(l)△H=-1225kJ/mol
| 化学键 | N-H | N-N | N≡N | O-H |
| 键能(kJ/mol) | 390 | 190 | 946 | 460 |