运用化学反应原理研究卤族元素的性质具有重要意义。
(1)下列关于氯水的叙述正确的是________(填写字母)。
a.氯水中存在两种电离平衡
b.向氯水中通入SO2,其漂白性增强
c.向氯水中通入氯气,c(H+)/c(ClO-)减小
d.加水稀释氯水,溶液中的所有离子浓度均减小
e.加水稀释氯水,水的电离平衡向正反应方向移动
f.向氯水中加入少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)常温下,已知25 ℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | HClO | H2CO3 |
| 电离平衡常数 | 4.7×10-8 | K1=4.3×10-7 K2=5.6×10-11 |
写出84消毒液露置在空气中发生反应的离子方程式
________________________________________________________________________
________________________________________________________________________。
(3)电解饱和食盐水可得到溶质为M的碱溶液,常温下将浓度为c1的M溶液与0.1 mol·L-1的一元酸HA等体积混合,所得溶液pH=7,则c1________0.1 mol·L-1(填“≥”、“=”或 “≤”),溶液中离子浓度的大小关系为______________________________。若将上述“0.1 mol·L-1的一元酸HA”改为“pH=1的一元酸HA”,所得溶液pH仍为7,则c1________0.1 mol·L-1。
(4)牙釉质对牙齿起着保护作用,其主要成分为羟基磷灰石,研究证实氟磷灰石比它更能抵抗酸的侵蚀,故含氟牙膏已使全世界千百万人较少龋齿,请写出羟基磷灰石的溶度积常数表达式Ksp=____________,氟离子与之反应转化的离子方程式为
________________________________________________________________________。
氯碱工业电解所用的氯化钠溶液需精制。除去有影响的Ca2+、Mg2+、NH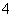 、SO
、SO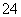 及泥沙,其精制流程如下:
及泥沙,其精制流程如下:
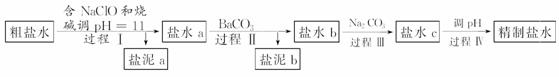 已知:①Ca2+、Mg2+开始形成相应氢氧化物沉淀的pH如下表。
已知:①Ca2+、Mg2+开始形成相应氢氧化物沉淀的pH如下表。
| Ca(OH)2 | Mg(OH)2 | |
| pH | ≥11.5 | ≥4.2 |
②Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=2.6×10-9,Ksp(CaCO3)=5.0×10-9。
下列说法正确的是( )
A.盐泥a除泥沙外,还含有Ca(OH)2和Mg(OH)2
B.过程Ⅰ中将NH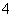 转化为N2的离子方程式是3ClO-+2NH
转化为N2的离子方程式是3ClO-+2NH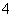 ===3Cl-+N2↑+3H2O+2H+
===3Cl-+N2↑+3H2O+2H+
C.过程Ⅱ中通入CO2有利于除SO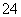
D.过程Ⅳ调pH可以使用硝酸
部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25 ℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
下列选项错误的是( )
①2CN-+H2O+CO2===2HCN+CO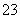
②2HCOOH+CO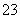 ===2HCOO-+H2O+CO2↑
===2HCOO-+H2O+CO2↑
③中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
④等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者
A.①② B.②③
C.③④ D.①④
甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使得甲醚在制药、燃料、农药等化学工业中有许多独特的用途。
(1)已知:2CH3OH(g)CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol·L-1) | 0.8 | 1.24 | ? |
①平衡时,c(CH3OCH3)等于________ mol·L-1,反应混合物的总能量减少________ kJ。
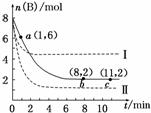
②若在平衡后的容器中再加入与起始时等量的CH3OH,请在下图中画出CH3OH的转化率和浓度的曲线示意图。

(2)在直接以甲醚为燃料的电池中,电解质溶液为酸性,负极的反应为________________、正极的反应为________________。
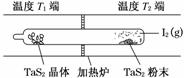
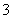 +H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=________mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中
+H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=________mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中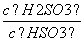 将________(填“增大”“减小”或“不变”)。
将________(填“增大”“减小”或“不变”)。
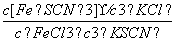
 (平衡常数为K3)。①、②、③的平衡常数关系为K1>K3>K2,据此所做的以下推测合理的是( )
(平衡常数为K3)。①、②、③的平衡常数关系为K1>K3>K2,据此所做的以下推测合理的是( )