常见离子共存情况剖析
| 常见离子组合 | 共存情况 | 原因 |
| (1)Ba2+、Ca2+与SO | ||
| CO | ||
| (2)Mg2+与SO | ||
| (3)OH-与NH | ||
| (4)OH-与Mg2+、Al3+、Fe2+ | ||
| (5)H+与CH3COO-、ClO-、 | ||
| HCO | ||
| (6)Fe3+、Al3+与CO | ||
| HCO | ||
| (7)NO | ||
| (8)Fe3+与S2-、I- | ||
| (9)MnO | ||
| (10)NH |
按要求回答下列问题:
⑴常温下,向VL 0.1mol/L的醋酸溶液中加水稀释,下列说法中正确的是 (填字母)
A.溶液中导电粒子的数目将减少 B.由水电离的c(H+)浓度将减小


C.溶液中不变 D.溶液中 将减小
E.醋酸的电离程度将增大,c(H+)也增大
⑵①常温下,将0.1mol/L的硫酸V1mL与0.1mol/LNaOH溶液V2mL混合后,溶液的pH=1则V1:V2= (忽略溶液体积的变化)。
②常温下,若溶液由pH=3的盐酸V1mL与pH=11的某碱BOH溶液V2mL混合而得,则下列假设和结论都正确的是 (填字母)
A.若混合后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol/L
B.若V1=V2,则混合后溶液的pH一定等于7
C.若V1=V2,则混合后一定有:c(Cl-)>c(B+)>c(H+)>c(OH-)
D.混合后的溶液中一定有c(B+)+c(H+)=c(Cl-)+c(OH-)
⑶常温下,浓度均为0.1mol/L的五种溶液的pH如下表所示:
| 溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①写出向NaClO溶液中通入少量CO2的离子方程式 。
②将浓度均为0.01mol/L下列溶液分别加水稀释10倍,pH变化最小的是 (填字母)
A.HCN B.HClO C.H2CO3 D.CH3COOH
③常温下,等浓度的醋酸与醋酸钠组成的混合溶液pH=6,则c(CH3COO-)-c(CH3COOH)=
(填准确数值)。
⑷已知常温下Ksp(AgCl)=1.0×10-10,Ksp (CH3COOAg)=9.0×10-4。常温下,CH3COOAg若要在NaCl溶液中开始转化为AgCl沉淀,则NaCl的浓度必须不低于 。
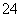 、
、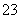 、SO
、SO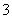
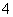 、HCO
、HCO



 2NH3(g) △H=-92kJ/mol。
2NH3(g) △H=-92kJ/mol。 。 CH3CH=CHCH3是石油裂解的产物之一,它的键线式结构可表示为
。 CH3CH=CHCH3是石油裂解的产物之一,它的键线式结构可表示为 。
。 是一种加聚产物,则其单体的结构简式为 ,其链节为
是一种加聚产物,则其单体的结构简式为 ,其链节为