恒温、恒容的条件下对于N2(g)+3H2(g)?2NH3(g)△H<0的反应,达到化学平衡状态的标志为( )
| A、断开一个N≡N键的同时有6个N-H键生成 |
| B、混合气体的密度不变 |
| C、混合气体的压强不变 |
| D、N2、H2、NH3分子数之比为1:3:2的状态 |
下列对有机物结构或性质的描述中错误的是( )
| A、一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 |
| B、乙烷和丙烯的物质的量共1mol,完成燃烧生成3mol H2O |
| C、用水可区分苯和溴苯 |
D、如图中有机物的一氯代物有4种 |
用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、T℃时,1 L pH=6纯水中,约含6.02×1017个OH- |
| B、6.8g熔融的KHSO4中含有6.02×1022个阳离子 |
| C、Na2O2与H2O反应,生成常温常压下16g O2,反应中转移电子数为2NA |
| D、用含有0.1mol FeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒个数等于0.1NA |
有关如图电化学装置的叙述中,正确的是( )


| A、若X为碳棒,Y为饱和食盐水,K置于N,则铁极上析出氯气 |
| B、若X为铂棒,Y为CuCl2溶液,K置于N,则铁棒质量将增加 |
| C、若X为锌棒,Y为海水,K置于M,形成对铁的外加电流阴极保护 |
| D、若X为铜棒,Y为稀硫酸,K置于M,则正极反应为:Fe-2e→Fe2+ |
下列实验中,溶液颜色有明显变化的是( )
| A、少量明矾溶液加入到过量NaOH溶液中 |
| B、往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 |
| C、少量Na2O2固体加入到过量NaHSO3溶液中 |
| D、往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3溶液 |
下列说法正确的是( )
A、金属的晶胞如图所示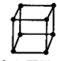 ,其配位数为8 ,其配位数为8 | ||||||||
| B、SO2分子中,S原子的价层电子对数为3,中心原子上孤电子对数为1,S原子为sp3杂化,是直线型分子 | ||||||||
| C、醋酸钠溶液中离子浓度的关系为:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | ||||||||
D、已知反应2CH3OH(g)?CH3OCH3+H2O(g),某温度下的平衡常数为400,此温度下,在恒容密闭容器中加入一定量CH3OH,某时刻测得各组分浓度如下表,则此时正、逆反应速率的大小关系为:v正>v逆
|
下列装置属于原电池的是( )
A、 稀硫酸 |
B、 酒精 |
C、 稀硫酸 |
D、 稀硫酸 |
某原电池的结构如图所示,下列有关该原电池的说法正确的是( )


| A、该电池工作时电能转变为化学能 |
| B、铜片的质量增加 |
| C、H+向铁片移动 |
| D、铁片上发生的反应是Fe-2e-═Fe2+ |
下列叙述正确的是( )
| A、常温常压下,4.6g NO2气体约含有1.81×1023个原子 |
| B、在标准状况下,80g SO3所占的体积约为22.4L |
| C、常温下,0.1mol?L-1醋酸溶液的pH约为1 |
| D、标准状况下,22.4L氯气与足量氢氧化钠溶液反应,转移的电子数为2NA |
设NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、标准状况下,22.4L Cl2完全溶于水时,转移电子数为NA |
| B、常温下,pH=1的H2SO4溶液中含有的H+的数目为0.1NA |
| C、标准状况下,2.24L SO3中含有硫原子的数目为NA |
| D、常温下,23g NO2和N2O4的混合气体中含有NA个氧原子 |