题目内容
设NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、标准状况下,22.4L Cl2完全溶于水时,转移电子数为NA |
| B、常温下,pH=1的H2SO4溶液中含有的H+的数目为0.1NA |
| C、标准状况下,2.24L SO3中含有硫原子的数目为NA |
| D、常温下,23g NO2和N2O4的混合气体中含有NA个氧原子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氯气溶于水中,只有少量的氯气与水反应生成氯化氢和次氯酸;
B.缺少硫酸溶液的体积,无法计算硫酸溶液中氢离子的数目;
C.标准状况下,三氧化硫的状态不是气体,不能使用标况下的气体摩尔体积计算三氧化硫的物质的量;
D.NO2和N2O4的最简式为NO2,根据最简式计算出混合物中含有氧原子的数目.
B.缺少硫酸溶液的体积,无法计算硫酸溶液中氢离子的数目;
C.标准状况下,三氧化硫的状态不是气体,不能使用标况下的气体摩尔体积计算三氧化硫的物质的量;
D.NO2和N2O4的最简式为NO2,根据最简式计算出混合物中含有氧原子的数目.
解答:
解:A.标况下22.4L氯气的物质的量为1mol,1mol氯气溶于水中,只有少量的氯气反应生成氯化氢和次氯酸,反应转移的电子小于1mol,转移电子数小于NA,故A错误;
B.没有告诉硫酸溶液的体积,无法计算硫酸溶液中氢离子的数目,故B错误;
C.标准状况下,三氧化硫不是气体,题中条件无法计算2.24L三氧化硫的物质的量,故C错误;
D.23g NO2和N2O4的混合气体中含有0.5mol最简式NO2,含有1mol氧原子,含有NA个氧原子,故D正确;
故选D.
B.没有告诉硫酸溶液的体积,无法计算硫酸溶液中氢离子的数目,故B错误;
C.标准状况下,三氧化硫不是气体,题中条件无法计算2.24L三氧化硫的物质的量,故C错误;
D.23g NO2和N2O4的混合气体中含有0.5mol最简式NO2,含有1mol氧原子,含有NA个氧原子,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意标准状况下三氧化硫的状态不是气体,要求掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项B为易错点,注意题中缺少硫酸溶液的体积.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列反应的离子方程式正确的是( )
| A、氢氧化铜和盐酸反应:OH-+H+═H2O |
| B、钠和水反应:Na+2H2O═Na++2OH-+H2↑ |
| C、铁和足量稀硝酸反应:Fe+2H+═Fe2++H2↑ |
| D、常温下,NaOH溶液和Cl2反应:2OH-+Cl2═Cl-+ClO-+H2O |
将纯锌片和纯铜片按如图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )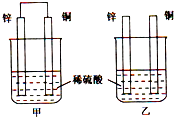

| A、两烧杯中铜片表面均无气泡产生 |
| B、甲中正极的电极反应式为Zn-2e-=Zn2+ |
| C、两烧杯中氢离子浓度均减少 |
| D、产生气泡的速度甲比乙慢 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温常压下,48g O2和O3组成的混和气体中所含的氧原子数为3NA |
| B、2mol H2O中含有36NA个电子 |
| C、2L 0.1mol?L-1 H2SO4溶液中含有0.2NA个H+ |
| D、常温常压下,22.4L CH4中含有NA个CH4分子 |
下列指定溶液中,各组离子可能大量共存的是( )
| A、pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
| B、在强酸溶液中:Na+、ClO-、Cl-、Ba2+ |
| C、在含有大量Fe3+的溶液中:NH4+、Cl-、Na+、SCN- |
| D、由水电离的c(H+)=10-13mol?L-1的溶液中:Mg2+、Cl-、K+、SO42- |
下列实验中,溶液颜色有明显变化的是( )
| A、少量明矾溶液加入到过量NaOH溶液中 |
| B、往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 |
| C、少量Na2O2固体加入到过量NaHSO3溶液中 |
| D、往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3溶液 |
下列表示物质结构的化学用语或模型图正确的是( )
| A、HClO的结构式:H-Cl-O |
B、NH3分子的电子式: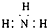 |
C、CO2的比例模型: |
D、18O的原子结构示意图: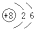 |
用加热的方法可以分离的一组物质是( )
| A、氯化铵和消石灰 |
| B、碳酸氢钠和氯化铵 |
| C、碳酸氢铵和过氧化钠 |
| D、氯化铵和氯化钠 |