题目内容
下列叙述正确的是( )
| A、常温常压下,4.6g NO2气体约含有1.81×1023个原子 |
| B、在标准状况下,80g SO3所占的体积约为22.4L |
| C、常温下,0.1mol?L-1醋酸溶液的pH约为1 |
| D、标准状况下,22.4L氯气与足量氢氧化钠溶液反应,转移的电子数为2NA |
考点:物质的量的相关计算
专题:计算题
分析:A.根据N=nNA=
NA结合分子构成计算原子个数;
B.标况下,三氧化硫是固体;
C.醋酸是弱电解质,在水溶液中存在电离平衡;
D.Cl2+2NaOH=NaCl+NaClO+H2O中氯气既是氧化剂又是还原剂,且氯气和转移电子之间的关系式为1:1.
| m |
| M |
B.标况下,三氧化硫是固体;
C.醋酸是弱电解质,在水溶液中存在电离平衡;
D.Cl2+2NaOH=NaCl+NaClO+H2O中氯气既是氧化剂又是还原剂,且氯气和转移电子之间的关系式为1:1.
解答:
解:A.二氧化氮能转化为四氧化二氮,四氧化二氮的相对分子质量、原子个数是二氧化氮的2倍,把气体当作二氧化氮计算即可,二氧化氮分子个数N=nNA=
NA=
×NA/mol=0.1NA,每个分子中含有3个原子,所以原子总数为1.81×1023,故A正确;
B.标况下,三氧化硫是固体,气体摩尔体积对其不适用,所以无法计算三氧化硫体积,故B错误;
C.醋酸是弱电解质,在水溶液中存在电离平衡,所以常温下,0.1mol?L-1醋酸溶液的pH大于1,故C错误;
D.Cl2+2NaOH=NaCl+NaClO+H2O中氯气既是氧化剂又是还原剂,且氯气和转移电子之间的关系式为1:1,标准状况下,22.4L氯气的物质的量为1mol,与足量氢氧化钠溶液反应,转移的电子数为NA,故D错误;
故选A.
| m |
| M |
| 4.6g |
| 46g/mol |
B.标况下,三氧化硫是固体,气体摩尔体积对其不适用,所以无法计算三氧化硫体积,故B错误;
C.醋酸是弱电解质,在水溶液中存在电离平衡,所以常温下,0.1mol?L-1醋酸溶液的pH大于1,故C错误;
D.Cl2+2NaOH=NaCl+NaClO+H2O中氯气既是氧化剂又是还原剂,且氯气和转移电子之间的关系式为1:1,标准状况下,22.4L氯气的物质的量为1mol,与足量氢氧化钠溶液反应,转移的电子数为NA,故D错误;
故选A.
点评:本题考查了物质的量的有关计算,涉及弱电解质的电离、物质之间的反应等知识点,注意A中即使二氧化氮转化为四氧化二氮也不改变原子个数,注意气体摩尔体积的适用范围及适用条件,为易错点.

练习册系列答案
相关题目
下列说法正确的是( )
| A、元素的单质可由氧化或还原含该元素的化合物来制得 |
| B、得电子越多的氧化剂,其氧化性就越强 |
| C、金属氧化物一定是碱性氧化物 |
| D、凡在溶液中能电离出H+的化合物都属于酸 |
加热固体试剂时,不能使用的仪器是( )
| A、试管 | B、烧杯 | C、燃烧匙 | D、坩埚 |
几种短周期元素的原子半径及主要化合价如表( )
下列叙述错误的是(其中NA表示阿伏加德罗常数的值)
| 元素代号 | X | Y | Z | M | N | P |
| 原子半径/nm | 0.186 | 0.143 | 0.075 | 0.074 | 0.152 | 0.099 |
| 元素的主要化合价 | +1 | +3 | +5、-3 | -2 | +1 | +7、-1 |
| A、X、N元素的金属性:X>N |
| B、Y、M元素形成的离子化合物是工业冶炼Y的原料 |
| C、X单质在M单质中燃烧生成的化合物39g中共含有0.5NA个阴离子 |
| D、标准状况下1L 1mol?L-1的YP3溶液中含有NA个Y3+离子 |
常温下,向100mL盐酸中滴加NaOH溶液,溶液的PH变化如图,由图可得出的正确结论是( )
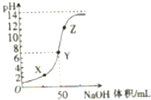

| A、原来盐酸的物质的量浓度为0.1 mol?L-1 |
| B、Y处溶液中只有两种离子 |
| C、原NaOH溶液的物质的量浓度为1 mol?L-1 |
| D、水的电离程度:X>Y>Z |
有关如图电化学装置的叙述中,正确的是( )


| A、若X为碳棒,Y为饱和食盐水,K置于N,则铁极上析出氯气 |
| B、若X为铂棒,Y为CuCl2溶液,K置于N,则铁棒质量将增加 |
| C、若X为锌棒,Y为海水,K置于M,形成对铁的外加电流阴极保护 |
| D、若X为铜棒,Y为稀硫酸,K置于M,则正极反应为:Fe-2e→Fe2+ |
下列化学过程及其表述正确的是( )
| A、向NaHSO4溶液中滴入Ba(OH)2溶液至中性H++SO42-+Ba2++OH═BaSO4↓+H2O |
| B、由水电离的c(H+)为10-3mol?L-1的溶液中,Na+、NO3-、SO32-、Cl-一定能大量共存 |
| C、向含有1mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总的物质的量为2mol |
| D、可以用浓盐酸酸化的KMnO4溶液与H2O2混合,以汪明H2O2具有还原性2MnO4+6H++5H2O2═2Mn2++5O2↑+8H2O |
2013年世界环境日中国主题为“同呼吸,共奋斗”.河南各地广泛开展了一系列活动.下列活动不符合这一主题的是( )
| A、推进以防治PM2.5为重点的大气污染防治工作 |
| B、积极推广风能、太阳能、氢能等新型能源的使用 |
| C、将生活垃圾、废品分类,实现资源再循环 |
| D、将高能耗、高污染的企业迁至偏僻的农村地区,提高当地居民收入 |
 右图是一个化学过程的示意图.已知甲池的总反应式为:
右图是一个化学过程的示意图.已知甲池的总反应式为: