题目内容
某原电池的结构如图所示,下列有关该原电池的说法正确的是( )
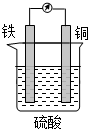

| A、该电池工作时电能转变为化学能 |
| B、铜片的质量增加 |
| C、H+向铁片移动 |
| D、铁片上发生的反应是Fe-2e-═Fe2+ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:该装置中,Fe易失电子作负极,铜作正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,溶液中阳离子向正极移动.
解答:
解:A.该装置为原电池,原电池工作时把化学能转化为电能,故A错误;
B.铜作正极,正极上氢离子得电子生成氢气,所以铜片的质量不变,故B错误;
C.溶液中阳离子向正极移动,所以H+向铜片移动,故C错误;
D.Fe易失电子作负极,铁片上发生的反应是Fe-2e-═Fe2+,故D正确;
故选D.
B.铜作正极,正极上氢离子得电子生成氢气,所以铜片的质量不变,故B错误;
C.溶液中阳离子向正极移动,所以H+向铜片移动,故C错误;
D.Fe易失电子作负极,铁片上发生的反应是Fe-2e-═Fe2+,故D正确;
故选D.
点评:本题考查了原电池原理,根据电极上得失电子判断正负极,再结合电极反应类型、离子流向来分析解答,熟记原电池原理,难点是电极反应式的书写.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
下列关于化石燃料及其加工说法正确的是( )
| A、天然气和沼气的主要成分都是甲烷,二者都是不可再生资源 |
| B、石油分馏和煤千馏都是物理变化,前者可得到汽油、煤油等,后者主要得到焦炭、煤焦油、粗氨水和焦炉气 |
| C、石油裂化主要是为了提高轻质油的产量,尤其是汽油的产量 |
| D、煤的液化指的是把煤加热到熔点以上使其变成液体 |
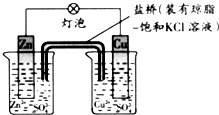 铜锌原电池工作时,下列叙述正确的是( )
铜锌原电池工作时,下列叙述正确的是( )| A、正极反应为:Zn-2e-=Zn2+ |
| B、在外电路中,电子从铜片流向锌片 |
| C、电池反应为:Zn+Cu2+=Zn2++Cu |
| D、盐桥中的K+移向ZnSO4溶液 |
下列反应离子方程式表示不正确的是( )
| A、NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O |
| B、Fe3O4与稀HNO3反应:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| C、向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| D、向次氯酸钠溶液中通入少量SO2:ClO-+SO2+H2O=Cl-+SO42-+2H+ |
下列离子方程式书写正确的是( )
| A、向KHSO4溶液中滴入Ba(OH)2溶液使pH=7:SO42-+H++Ba2++OH-=BaSO4↓+H2O |
| B、少量小苏打溶液滴入Ba(OH)2溶液中:HCO3-+Ba2++OH-=BaCO3↓+H2O |
| C、硫氢化钠发生水解:HS-+H2O?H3O++S2- |
| D、FeS固体加入到用硫酸酸化的H2O2溶液中:2Fe2++2H++H2O2=2Fe3++2H2O |
用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、T℃时,1 L pH=6纯水中,约含6.02×1017个OH- |
| B、6.8g熔融的KHSO4中含有6.02×1022个阳离子 |
| C、Na2O2与H2O反应,生成常温常压下16g O2,反应中转移电子数为2NA |
| D、用含有0.1mol FeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒个数等于0.1NA |
在100mL 1.0mol/L的AlCl3溶液中加入350mL 1.0mol/L的NaOH溶液充分反应后,得到的沉淀的质量是( )
| A、7.8g | B、3.9g |
| C、15.6g | D、无沉淀 |
下列各组离子在给定条件下能大量共存的是( )
| A、能使pH试纸呈红色的溶液:Na+、NH4+、Cl-、NO3- |
| B、滴入KSCN溶液显血红色的溶液:K+、Na+、CO32-、I- |
| C、能与铝反应产生H2的溶液:K+、Fe2+、Cl-、NO3- |
| D、常温下由水电离出的c(H+)=1×10-13mol/L的溶液:HCO3-、K+、SO42-、Cl- |