下列离子方程式中正确的是( )
| A、碳酸氢铵溶液与足量苛性钾溶液混合共热:NH4++OH-=NH3↑+H2O |
| B、Fe3O4溶解在过量的稀硝酸中:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| C、往硫酸铜溶液中加入过量的NaHS溶液:Cu2++2HS-=CuS↓+H2S↑ |
| D、石灰石溶解在醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
下列对于“摩尔”的理解正确的是( )
| A、摩尔是国际科学界建议采用的一种物理量 |
| B、32g O2中所含氧原子数为NA个 |
| C、1mol氧约含6.02×1023个O2 |
| D、摩尔是物质的量的单位,简称摩,符号为mol |
下列说法正确的是( )
| A、发生化学反应时失去电子越多的金属原子,还原能力越强 |
| B、金属阳离子被还原后,不一定得到该元素的单质 |
| C、核外电子总数相同的粒子,一定是同种元素的原子 |
| D、只能与酸反应的氧化物,一定是碱性氧化物 |
下列说法正确的是( )
| A、金属钠着火可用煤油扑灭 |
| B、将几滴FeCl3饱和溶液滴入氢氧化钠溶液可制备Fe(OH)3胶体 |
| C、向含有等量NaI、NaCl的溶液中滴加AgNO3溶液,先产生白色沉淀 |
| D、用浓氢氧化钠溶液和湿润红色石蕊试纸检验某溶液中是否有NH4+ |
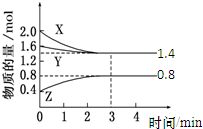 t℃时,在容积为2L密闭中充入X(g)、Y(g)与Z(g),反应过程中X、Y、Z的物质的量变化如下图所示.下列说法不正确的是( )
t℃时,在容积为2L密闭中充入X(g)、Y(g)与Z(g),反应过程中X、Y、Z的物质的量变化如下图所示.下列说法不正确的是( )| A、0~3 min,X的平均反应速率v(X)=0.2 mol?L-1?min-1 |
| B、发生反应的方程式可表示为:3X(g)+Y(g)?2Z(g) |
| C、保持其他条件不变,增大压强,平衡向正反应方向移动 |
| D、温度不变,增大X的浓度,该反应的平衡常数不变 |
若某电能与化学能的转化装置(电解池或原电池)中发生的总反应的离子方程式是Cu+2H+═Cu2++H2↑,则下列关于该装置的有关说法中正确的是( )
| A、该装置可能是原电池,可用Cu、C作电极,电解质溶液是盐酸 |
| B、该装置可能是原电池,电解质溶液为硝酸 |
| C、该装置只能是电解池,金属铜为该电解池的阳极,K2SO4为电解质溶液 |
| D、该装置只能是电解池,金属铜为该电解池的阳极,稀H2SO4为电解质溶液 |
下列变化不属于化学变化的是( )
| A、次氯酸钠使有色布条褪色 |
| B、氯水使用色花辨褪色 |
| C、活性炭使红墨水褪色 |
| D、H2O2水溶液使染料褪色 |
将0.5mol Na投入过量的水(m1g)中,得到a g溶液;将0.5mol Zn投入过量的盐酸(m2g)中,得到bg溶液,若m1═m2,则a.b的质量关系是( )
| A、a>b | B、a<b |
| C、a=b | D、不能确定 |
对于可逆反应H2(g)+I2(g)?2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是( )
| A、H2(g)的消耗速率与HI(g)的生成速率之比为2:1 |
| B、若平衡正向移动,则V正一定增大 |
| C、正、逆反应速率的比值是恒定的 |
| D、达到平衡时,正、逆反应速率相等 |
下列有关叙述错误的是( )
A、水分子的结构式为  |
| B、氧与氟形成的化合物(OF2)中,氧元素的化合价为-2价 |
C、Na2O2的电子式为Na+ Na+ Na+ |
D、在MgO晶体中,O2-的结构示意图可表示为 |